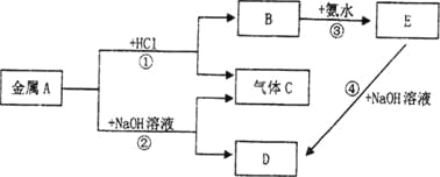
题目内容
【题目】A、B、C、D均为短周期元素,A和B是同周期相邻的两种元素,A和C是同主族相邻的两种元素,A、B、C三种元素的原子序数之和为31,D元素与A、B、C三种元素既不同周期,也不同主族,请回答:
(1)C元素在元素周期表中的位置是_____________________________;
(2)A、B、D可组成一种离子化合物,是常见的化肥,其化学式为_________________;
(3)A2和D2两种物质可以构成一种新型的原电池,若原电池中电解质溶液为KOH溶液,则正极的电极反应式为_____________________________;
(4)若将一充满20 mlBA2和A2混合气体的大试管倒立于D2A中,充分反应后,在相同条件下,测得试管中余下5mL无色气体,则原混合气体中BA2和A2物质的量之比为________________。
【答案】 第三周期第ⅥA族 NH4NO3 O2 + 2H2O + 4e- = 4OH- 3︰2 或 19︰1
【解析】A、B、C、D均为短周期元素,A和B是同周期相邻的两种元素,A和C是同主族相邻的两种元素:A、B、C三种元素的原子序数之和为31,则A、B、C可能有如下几种相对位置: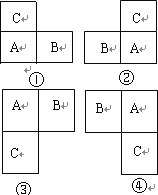
①设A的原子序数为x,则C为x-8,B为x+1,则x+x-8+x+1=31,解之得:x=![]() ,不符合题意;②设A的原子序数为x,则C为x-8,B为x-1,则x+x-8+x-1=31,解之得:x=
,不符合题意;②设A的原子序数为x,则C为x-8,B为x-1,则x+x-8+x-1=31,解之得:x=![]() ,不符合题意;③设A的原子序数为x,则C为x+8,B为x+1,则x+x+8+x+1=31,解之得:x=
,不符合题意;③设A的原子序数为x,则C为x+8,B为x+1,则x+x+8+x+1=31,解之得:x=![]() ,不符合题意;④设A的原子序数为x,则C为x+8,B为x-1,则x+x+8+x-1=31,解之得:x=8,则A为O元素,B为N元素,C为S元素,D元素与A、B、C三种元素既不是同周期,也不同主族,且为短周期元素,应为H元素;
,不符合题意;④设A的原子序数为x,则C为x+8,B为x-1,则x+x+8+x-1=31,解之得:x=8,则A为O元素,B为N元素,C为S元素,D元素与A、B、C三种元素既不是同周期,也不同主族,且为短周期元素,应为H元素;
(1)S元素在元素周期表中的位置是第三周期第ⅥA族;
(2)N、O、H组成的一种离子化合物,且是常见的化肥,其化学式为NH4NO3;
(3)O2和H2两种物质可以构成一种新型的原电池,若原电池中电解质溶液为KOH溶液,通O2的极为正极,发生还原反应,此电极反应式为O2 + 2H2O + 4e- = 4OH- ;
(4)可能发生的反应为:4NO2+O2+2H2O=4HNO3,3NO2+H2O=2HNO3+NO,剩余气体为NO或氧气,若为氧气,则参加反应的气体为20mL-5mL=15mL,根据4NO2+O2+2H2O=4HNO3,可知参加此反应的NO2的体积为15ml×![]() =12mL,则原混合气体中NO2和O2物质的量之比为12mL:8mL=3:2;若剩余气体为NO气体,根据3NO2+H2O=2HNO3+NO,可知过量的NO2为3×5mL=15mL,反应4NO2+O2+2H2O=4HNO3消耗的气体总体积为20mL-15mL=5mL,则反应消耗的二氧化氮为5mL×
=12mL,则原混合气体中NO2和O2物质的量之比为12mL:8mL=3:2;若剩余气体为NO气体,根据3NO2+H2O=2HNO3+NO,可知过量的NO2为3×5mL=15mL,反应4NO2+O2+2H2O=4HNO3消耗的气体总体积为20mL-15mL=5mL,则反应消耗的二氧化氮为5mL×![]() =4mL,则原混合气体中的NO2的体积为4+15=19mL,原混合气体中NO2和O2物质的量之比为19mL:1mL=19:1。
=4mL,则原混合气体中的NO2的体积为4+15=19mL,原混合气体中NO2和O2物质的量之比为19mL:1mL=19:1。

 名校通行证有效作业系列答案
名校通行证有效作业系列答案