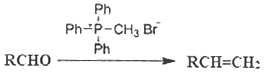
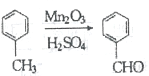
题目内容
【题目】在一定的温度下,向一个容积为2 L的恒容密闭容器中(事先装入催化剂),充入2molN2和3molH2, 3min后测得密闭容器内的压强是起始时的0.9倍。在这段时间内,用H2表示该反应的平均反应速率是
A. 0.125mol·L-1·min-1 B. 0.100 mol·L-1·s-1
C. 0.200 mol·L-1·min-1 D. 0.375 mol·L-1·s-1
【答案】A
【解析】3min末测得容器内压强是起始时压强的0.9倍,压强之比等于物质的量之比,
所以3min末时容器内混合气体的物质的量为(2mol+3mol)×0.9=4.5mol
3H2+N2 ![]() 2NH3 物质的量变化 △n
2NH3 物质的量变化 △n
3 2
△n(H2)5mol-4.5mol=0.5mol
所以△n(H2)= ![]() ×0.5mol=0.75mol,
×0.5mol=0.75mol,
所以3min内,用H2表示的平均反应速率v(H2)=  = 0.125mol·L-1·min-1 ;故答案为A。
= 0.125mol·L-1·min-1 ;故答案为A。

 备战中考寒假系列答案
备战中考寒假系列答案【题目】汽车排放的尾气为大气污染源之一,目前,可利用以下化学原理解决尾气:2NO+2CO![]() 2CO2+N2。
2CO2+N2。
(1)写出CO2的结构式____________,N2的电子式___________。
(2)一定条件下,在容积固定的容器中进行上述反应,CO浓度与时间关系如图所示:
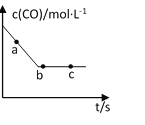
①则反应速率υ(a)、υ(b)、 υ(c)的大小关系是______________;
②下列可说明反应到达图中c点的是__________;
A.NO、CO、CO2、N2表示的速率比值保持2︰2︰2︰1不变
B.CO的浓度不再改变
C.反应消耗2molNO的同时消耗1molN2
D.容器中的气体质量或物质的量保持不变
(3)为研究如何提高该转化过程反应速率,某课题组进行了以下实验探究。
【资料查阅】
A.不同的催化剂对同一反应的催化效率不同;
B.使用等质量相同的催化剂时,催化剂的比表面积对催化效率有影响。
【实验设计】课题组为探究某些外界条件对汽车尾气转化反应速率的影响规律,设计了以下对比实验。
实验编号 | 实验目的 | T/℃ | NO初始浓度 mol/L | CO初始浓度 mol/L | 同种催化剂的比表面积 m2/g | 达平衡时所用的时间min |
Ⅰ | 参照实验 | 280 | 6.50×10-3 | 4.00×10-3 | 80 | t |
Ⅱ | 280 | 6.50×10-3 | 4.00×10-3 | 120 | 0.5t | |
Ⅲ | 360 | 6.50×10-3 | 4.00×10-3 | 80 | 0.2t |
【结论】①实验编号Ⅱ的实验目的为_________________________。
②课题中探究外界条件对汽车尾气转化反应速率的影响的另一因素是___________,且____________反应速率将___________。(填“增大”、“减小”、“无影响”)。