题目内容
19.下列说法正确的是( )| A. | 银氨溶液可用于检验淀粉是否发生水解 | |
| B. | 植物油的主要成分是高级脂肪酸 | |
| C. | 蔗糖及其水解产物均可发生银镜反应 | |
| D. | 鸡蛋清溶液中加入饱和硫酸钠溶液,生成的沉淀物不能再溶解 |
分析 A.淀粉水解生成葡萄糖,葡萄糖可与银氨溶液发生银镜反应;
B.植物油为油脂;
C.蔗糖不含-CHO,水解生成葡萄糖含-CHO;
D.鸡蛋清溶液中加入饱和硫酸钠溶液,发生盐析.
解答 解:A.淀粉水解生成葡萄糖,葡萄糖可与银氨溶液发生银镜反应,则银氨溶液可用于检验淀粉是否发生水解,故A正确;
B.植物油为油脂,其成分为高级脂肪酸甘油酯,故B错误;
C.蔗糖及其水解产物中,只有葡萄糖可发生银镜反应,故C错误;
D.鸡蛋清溶液中加入饱和硫酸钠溶液,发生盐析,为可逆过程,则生成的沉淀物能再溶解,故D错误;
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、组成和性质等为解答的关键,注意葡萄糖、油脂、蛋白质的性质,综合性较强,注重基础知识的考查,题目难度不大.

练习册系列答案
 小学课时特训系列答案
小学课时特训系列答案
相关题目
9.从金属利用的历史来看,先是青铜器时代,而后是铁器时代,铝的利用是近百年的事.这个先后顺序跟下列有关的是:①地壳中的金属元素的含量;②金属活动性;③金属的导电性;④金属冶炼的难易程度;⑤金属的延展性( )
| A. | ①③ | B. | ②④ | C. | ③⑤ | D. | ②⑤ |
10.设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 1.7g OH- 所含电子数为0.9NA | |
| B. | 标准状况下,11.2 L HCl 所含质子数为18NA | |
| C. | 7.8gNa2O2固体中含有的离子数为4NA | |
| D. | 0.5 mol D2O 中所含质子数为5NA |
14.下列有关说法正确的是( )
| A. | 马口铁(镀锡铁)镀层受损后,铁制品比受损前更容易生锈 | |
| B. | 2CaCO3(s)+2SO2(g)+O2(g)═2CaSO4(s)+2CO2(g)在高温下能自发进行,则该反应的△H>0 | |
| C. | 恒温恒容密闭容器中进行的反应N2(g)+3H2(g)?2NH3(g);△H=a kJ•mol-1,平衡时向容器中再充入N2和H2,反应速率加快,a值不变 | |
| D. | 氢硫酸(弱酸)中加入少量CuSO4溶液(H2S+CuSO4═CuS↓+H2SO4),H2S的电离程度和溶液的pH均增大 |
4.设NA表示阿伏加德罗常数的值,下列有关NA的叙述中正确的是( )
| A. | 惰性电极电解饱和食盐水,若电路中通过NA个电子,则阳极产生气体11.2L | |
| B. | 标准状况下,4.0 g CH4中含有共价键的数目为NA | |
| C. | 1 mol C12发生化学反应,转移的电子数必为2NA | |
| D. | 在反应KIO3+6HI=KI+3I2+3H2O中,每生成3mol I2转移的电子数为6NA |
11.下列关于有机物的说法正确的是( )
| A. | 乙烯和苯都能使溴水褪色,褪色的原因相同 | |
| B. | 甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应 | |
| C. | 葡萄糖和果糖的分子式均为C6H12O6,二者互为同系物 | |
| D. | 乙醇、乙酸、乙酸乙酯都能发生取代反应,乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去 |
8.一定温度下,向a L密闭容器中加入2mol NO2(g),发生反应:2NO2?2NO+O2,此反应达到平衡状态时的标志是( )
| A. | 混合气体的颜色变浅 | |
| B. | 混合气体的密度不再变化 | |
| C. | 混合气体中NO2、NO、O2物质的量之比为2:2:1 | |
| D. | 单位时间内生成2n mol NO,同时生成2n mol NO2 |
9.化学与社会、生产、生活密切相关,下列说法正确的是( )
| A. | 氢氧化铝、氢氧化钠、碳酸钠都是常见的胃酸中和剂 | |
| B. | 研发易降解的生物农药有利于环境保护 | |
| C. | 做衣服的棉、麻、蚕丝的成分都是纤维素 | |
| D. | 常用无水酒精来消毒,是因为酒精能够使细菌蛋白发生变性 |
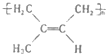 :其1mol单体跟1molBr2发生加成反应生成的产物有3种;
:其1mol单体跟1molBr2发生加成反应生成的产物有3种;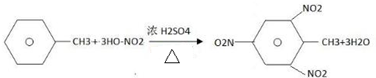 .
.