题目内容
9.从金属利用的历史来看,先是青铜器时代,而后是铁器时代,铝的利用是近百年的事.这个先后顺序跟下列有关的是:①地壳中的金属元素的含量;②金属活动性;③金属的导电性;④金属冶炼的难易程度;⑤金属的延展性( )| A. | ①③ | B. | ②④ | C. | ③⑤ | D. | ②⑤ |
分析 金属的活泼性越强,金属越容易被氧化,越不稳定,在自然界中越容易以化合态存在,金属的冶炼越难,据此分析解答.
解答 解:铜、铁、铝三种金属活动性由强到弱的顺序为:铝>铁>铜,金属的活泼性越强,金属越容易被氧化,越不稳定,在自然界中越容易以化合态存在,金属的冶炼越难,所以金属的使用早晚与金属的活动性强弱、金属的冶炼难易程度有关,
故选:B.
点评 本题考查了金属活泼性与使用早晚的关系,明确金属活泼性与金属冶炼难易之间的关系是解题关键,题目难度不大.

练习册系列答案
相关题目
20.下列反应过程中能量变化符合如图所示的是( )
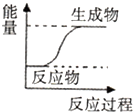

| A. | C+C02 $\frac{\underline{\;高温\;}}{\;}$2CO | B. | Zn+H2S04=ZnS04+H2↑ | ||
| C. | CH4+202$\stackrel{点燃}{→}$C02+2H20 | D. | K0H+HN03=KN03+H20 |
17.下列物质的电子式书写正确的是( )
| A. | 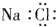 | B. |  | C. |  | D. | 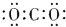 |
4.NH5属于离子化合物,与水反应的化学方程式为:NH5+H2O=NH3.H2O+H2↑,有关NH5叙述正确的是( )
| A. | NH5的电子式: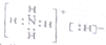 | |
| B. | NH5中N元素的化合价为+5价 | |
| C. | 1molNH5中含有5molN-H键 | |
| D. | 1molNH5与H2O完全反应,转移电子2mol |
14.向明矾[KAl(SO4)2•12H2O]溶液中滴加Ba(OH)2溶液,当SO42-完全沉淀时,铝元素的存在形式是( )
| A. | 全部为Al(OH)3沉淀 | |
| B. | 几乎全部以AlO2-形式存在于溶液中 | |
| C. | 一部分为Al(OH)3沉淀,一部分以Al3+存在于溶液中 | |
| D. | 一部分为Al(OH)3沉淀,一部分以AlO3-形式存在于溶液中 |
18.为进行Ⅰ项中的除杂实验(括号内为杂质),请从Ⅱ项中选出一种试剂,从Ⅲ项中选出一合适的实验操作方法分离,将标号填在后面的答案栏内.
| Ⅰ除杂实验 | Ⅱ试剂 | Ⅲ操作方法 | 答案 | ||
| Ⅰ | Ⅱ | Ⅲ | |||
| ①苯(苯酚) | A.饱和Na2CO3溶液 B.NaOH溶液 C.CaO | a.过滤 b.蒸馏 c.分液 | ① | ||
| ②乙醇(水) | ② | ||||
| ③乙酸乙酯(乙酸) | ③ | ||||
19.下列说法正确的是( )
| A. | 银氨溶液可用于检验淀粉是否发生水解 | |
| B. | 植物油的主要成分是高级脂肪酸 | |
| C. | 蔗糖及其水解产物均可发生银镜反应 | |
| D. | 鸡蛋清溶液中加入饱和硫酸钠溶液,生成的沉淀物不能再溶解 |

 ,B、C可形成离子化合物B3C2,E是同周期元素中原子半径最小的元素.
,B、C可形成离子化合物B3C2,E是同周期元素中原子半径最小的元素. .
.