题目内容
【题目】工业产生的废气COx、NOx、SOx对环境有害,若能合理的利用吸收,可以减少污染,变废为宝。
(1)已知甲烷的燃烧热为890 kJ/mol;1 mol水蒸气变成液态水放热44 kJ;N2与O2反应生成NO的过程如下:
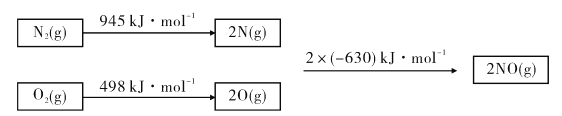
则CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=_______.
(2)汽车尾气中含有CO和NO,某研究小组利用反应:2CO(g)+2NO(g) ![]() N2 (g)+2CO2 (g)实现气体的无害化排放。T1℃时,在恒容的密闭容器中通入一定量的CO和NO,能自发进行上述反应,测得不同时间的NO和CO的浓度如下表:
N2 (g)+2CO2 (g)实现气体的无害化排放。T1℃时,在恒容的密闭容器中通入一定量的CO和NO,能自发进行上述反应,测得不同时间的NO和CO的浓度如下表:
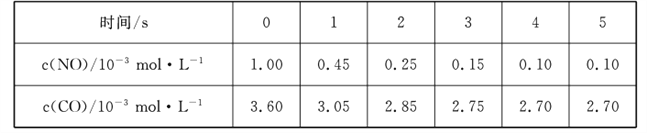
①0~2 s内用N2表示的化学反应速率为____,该温度下,反应的平衡常数K1_____。
②若该反应在绝热恒容条件下进行,则反应达到平衡后体系的温度为T2℃,此时的化学平衡常数为K2,则K1____K2(填“>”、“<”或“=”),原因是________
(3)向甲、乙两个容积均为1 L的恒温恒容的密闭容器中,分别充入一定量的SO2和O2(其中,甲充入2 mol SO2、1 mol O2,乙充入1 mol SO2、0.5 mol O2),发生反应:2SO2(g)+O2 (g) ![]() 2SO3 (g) △H= -197. 74 kJ/mol ,一段时间后达到平衡,测得两容器中c(SO2)(mol/L)随时间t(min)的变化关系如右图所示。下列说法正确的是______
2SO3 (g) △H= -197. 74 kJ/mol ,一段时间后达到平衡,测得两容器中c(SO2)(mol/L)随时间t(min)的变化关系如右图所示。下列说法正确的是______
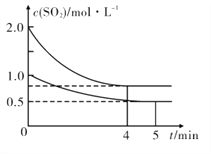
A.放出的热量Q:Q(甲)>2Q(乙)
B.体系总压强p:p(甲)>2p(乙)
C.甲容器达到化学平衡时,其化学平衡常数为4
D.保持其他条件不变,若起始时向乙中充入0.4 mol SO2、0.2mol O2、0.4 molSO3,则此时v(正>v(逆)
(4)在强酸性的电解质水溶液中,惰性材料做电极,电解CO2可得到多种燃料,其原理如右图所示。
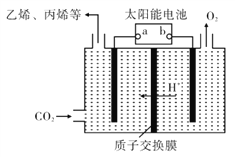
①该工艺中能量转化方式主要有____。
②电解时,生成乙烯的电极反应式是____。
(5)CO2在自然界循环时可与CaC03反应,Ca-CO3是一种难溶物质,其Ksp=2.8×10-9。CaCl2溶液与Na2 CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2 CO3溶液混合,若Na2 C03溶液的浓度为2×10-4 mol/L,则生成沉淀所需CaCl2溶液的最小浓度为_________。
【答案】 -612 kJ·mol-1 1.875×10-4mol/(L·s) 5000 > 2CO+2NO![]() N2+2CO2 的△S<0,只有当△H<0,时△G=△H-T△S才能小于0,反应才能在一定条件下自发进行,所以该反应为放热反应。若该反应在绝热恒容条件下进行,由于初始时只有反应物,反应一定正向进行,达到平衡后反应体系温度升高,所以T1<T2,对于放热反应,温度升高,平衡初始减小,所以K1>K2 AC 太阳能转化为电能;电能转化为化学能
N2+2CO2 的△S<0,只有当△H<0,时△G=△H-T△S才能小于0,反应才能在一定条件下自发进行,所以该反应为放热反应。若该反应在绝热恒容条件下进行,由于初始时只有反应物,反应一定正向进行,达到平衡后反应体系温度升高,所以T1<T2,对于放热反应,温度升高,平衡初始减小,所以K1>K2 AC 太阳能转化为电能;电能转化为化学能 ![]() 5.6×10—5mo1/L
5.6×10—5mo1/L
【解析】(1)根据图示,旧键断裂吸收能量为:945+498=1443KJ/mol,放出能量为:2×630=1260KJ/mol,则热化学方程式为2NO(g)=O2(g)+N2(g)△H=-1260+1443=183KJ/mol①;甲烷燃烧热为890kJ/mol,可写出热化学方程式为CH4(g)+2O2(g)=CO2(g)+2H2O(l),△H=-890kJ/mol②;H2O(g)=H2O(l),△H=-44kJ/mol③;由盖斯定律可知②+①×2-③×2,可得CH4 (g) +4NO(g)=2N2 (g) +CO2 (g) +2H2 O(g) △H=-890kJ/mol+183/mol×2-(44kJ/mol)×2=-612kJmol-1,故答案为:-612kJmol-1;
(2) ①前2s内的平均反应速率v(N2)= ![]() v(N0)=
v(N0)= ![]() ×
×![]() =1.875×10-4mol/(L·s),由表格中的数据可知到4s时达到化学平衡,则
=1.875×10-4mol/(L·s),由表格中的数据可知到4s时达到化学平衡,则
2NO + 2CO![]() 2CO2 + N2,
2CO2 + N2,
开始(mol/L) 1.00×10-3 3.60×10-3 0 0
转化(mol/L) 9×10-4 9×10-4 9×10-4 4.50×10-4
平衡(mol/L) 1.00×10-4 2.70×10-3 9×10-4 4.50×10-4
则 K=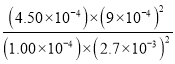 =5000,故答案为:1.875×10-4mol/(L·s);5000
=5000,故答案为:1.875×10-4mol/(L·s);5000
②2CO+2NO![]() N2+2CO2 的△S<0,只有当△H<0,时△G=△H-T△S才能小于0,反应才能在一定条件下自发进行,所以该反应为放热反应。若该反应在绝热恒容条件下进行,由于初始时只有反应物,反应一定正向进行,达到平衡后反应体系温度升高,所以T1<T2,对于放热反应,温度升高,平衡初始减小,所以K1>K2 ,故答案为:> ;2CO+2NO
N2+2CO2 的△S<0,只有当△H<0,时△G=△H-T△S才能小于0,反应才能在一定条件下自发进行,所以该反应为放热反应。若该反应在绝热恒容条件下进行,由于初始时只有反应物,反应一定正向进行,达到平衡后反应体系温度升高,所以T1<T2,对于放热反应,温度升高,平衡初始减小,所以K1>K2 ,故答案为:> ;2CO+2NO![]() N2+2CO2 的△S<0,只有当△H<0,时△G=△H-T△S才能小于0,反应才能在一定条件下自发进行,所以该反应为放热反应。若该反应在绝热恒容条件下进行,由于初始时只有反应物,反应一定正向进行,达到平衡后反应体系温度升高,所以T1<T2,对于放热反应,温度升高,平衡初始减小,所以K1>K2;
N2+2CO2 的△S<0,只有当△H<0,时△G=△H-T△S才能小于0,反应才能在一定条件下自发进行,所以该反应为放热反应。若该反应在绝热恒容条件下进行,由于初始时只有反应物,反应一定正向进行,达到平衡后反应体系温度升高,所以T1<T2,对于放热反应,温度升高,平衡初始减小,所以K1>K2;
(3)A.该反应反应前气体体积大于反应后体积,即充入反应物物质的量越大则压强越大,进行程度较大,放出热量Q(甲)>2Q(乙),故A正确;B.该反应反应前气体体积大于反应后体积,即充入反应物物质的量越大则压强越大,进行程度较大,则压强p(甲)<2p(乙),故B错误;C.乙容器达到化学平衡状态时,c(SO2)=0.5mol/L,c(O2)=0.5mol/L-0.5mol/L×![]() =0.25mol/L,c(SO3)=0.5mol/L,K=
=0.25mol/L,c(SO3)=0.5mol/L,K=![]() =4,故C正确;D.浓度商为:
=4,故C正确;D.浓度商为: ![]() =5,浓度商大于化学平衡常数,化学平衡向逆反应方向移动,即v(正)<v(逆),故D错误;故选AC;
=5,浓度商大于化学平衡常数,化学平衡向逆反应方向移动,即v(正)<v(逆),故D错误;故选AC;
(4)①太阳能电池为电源,电解强酸性的二氧化碳水溶液得到乙烯,可知能量转化形式有光能转化为电能,电能转化为化学能,部分电能转化为热能,故答案为:太阳能转化为电能,电能转化为化学能;
②电解时,二氧化碳在b极上生成乙烯,电极反应式为2CO2+12H++12e-=C2H4+4H2O,故答案为:正;2CO2+12H++12e-=C2H4+4H2O;
(5)Na2CO3溶液的浓度为2×10-4mol/L,等体积混合后溶液中c(CO32-)=![]() ×2×10-4mol/L=1×10-4mol/L,根据Ksp=c(CO32-)c(Ca2+)=2.8×10-9可知,c(Ca2+)=
×2×10-4mol/L=1×10-4mol/L,根据Ksp=c(CO32-)c(Ca2+)=2.8×10-9可知,c(Ca2+)=![]() mol/L=2.8×10-5mol/L,原溶液CaCl2溶液的最小浓度为混合溶液中c(Ca2+)的2倍,故原溶液CaCl2溶液的最小浓度为2×2.8×10-5mol/L=5.6×10-5mol/L,故答案为:5.6×10-5 mo1/L。
mol/L=2.8×10-5mol/L,原溶液CaCl2溶液的最小浓度为混合溶液中c(Ca2+)的2倍,故原溶液CaCl2溶液的最小浓度为2×2.8×10-5mol/L=5.6×10-5mol/L,故答案为:5.6×10-5 mo1/L。

 阅读快车系列答案
阅读快车系列答案【题目】盐在化学工业中有重要的应用,请回答下列问题。
(1)用离子方程式表示FeCl3可作净水剂的原因:______________________________。
(2)常温下,在pH=3的硫酸与pH =11的Na2S溶液中,水电离出来的c(OH-)之比为_______
(3)物质的量浓度相等的下列溶液①NH4Cl②NH4 HSO4③(NH4 ) 2SO4④CH3 COONH4⑤NH3 H2O,溶液中的C(NH4 +)由大到小的顺序是__________________(用序号表示)。
(4)25℃,两种酸的电离平衡常数如下表:
Ka1 | Ka2 | |
H2SO3 | 1.3x10-2 | 6.3x10-8 |
H2CO3 | 4.2x10-7 | 5.6x10-11 |
①0.10 mol L-1NaHSO3溶液中离子浓度由大到小的顺序为__________________
②向NaHCO3溶液中通入少量二氧化硫时反应的离子方程式为__________________________
(5)已知 25 ℃ 时 Ksp[Mg(OH)2] =1.8×10-11, Ksp[Cu(OH)2] =2.2 ×10-20.25 ℃时,向浓度均为0.1 mol L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成________(填化学式)沉淀;当体系中两种沉淀共存时,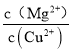 =_______。
=_______。
【题目】Ⅰ.现有下列仪器或用品:①铁架台(含铁圈、各式铁夹) ②锥形瓶 ③酸式滴定管和碱式滴定管 ④烧杯 ⑤玻璃棒 ⑥胶头滴管 ⑦天平(含砝码) ⑧滤纸 ⑨量筒 ⑩过滤漏斗;
现有下列药品:(A)NaOH固体 (B)标准NaOH溶液(C)未知浓度盐酸 (D)蒸馏水(E)碳酸钠溶液
根据所做过的学生实验,回答下列问题:
(1)过滤时,应选用的上述仪器是_________________________(填编号)。
(2)配制一定物质的量浓度的NaOH溶液时,还缺少的仪器是__________。
(3)做酸碱中和滴定时,还缺乏的试剂是____________________。
(4)进行中和滴定时,绝不可用将要盛的溶液事先润洗的仪器是下列的______(填编号)。甲.酸式滴定管 乙.碱式滴定管 丙.锥形瓶
(5)用标准的NaOH溶液滴定未知浓度的盐酸,选用酚酞作为指示剂,造成测定结果偏高的原因可能是______________。
A.配制标准溶液的NaOH中混有Na2CO3杂质
B.滴定终点读数时,俯视滴定管的刻度,其他操作正确
C.盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗
D.滴定前有气泡,滴定后气泡消失。
II. 甲醇(CH3OH)是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应I:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH1
CH3OH(g)+H2O(g) ΔH1
反应II:CO(g)+2H2(g)![]() CH3OH(g) ΔH2
CH3OH(g) ΔH2
①反应I的平衡常数表达式为K=________________________
②下表所列数据是反应Ⅱ在不同温度下的化学平衡常数(K)
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
由表中数据判断ΔH2______0,ΔS______0 (填“>”、“=”或“<”=)。
③某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2 mol·L-1,则CO的转化率为________。
(2)已知在常温常压下,某实验小组依据甲醇燃烧的反应原理,设计如下图所示的电池装置:

①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH =-1275.6 kJ·mol-1
②H2O(g)=H2O(l) ΔH =-44.0 kJ·mol-1
①写出表示甲醇燃烧热的热化学方程式____________________。
②写出上图电池装置中负极反应式:________________________________。
【题目】工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大损害,要进行必要的处理。
两种离子在溶液中存在如下平衡:2CrO42-(黄色)+2H+![]() Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O
现对某工业废水进行检测并做沉降处理,请回答下列问题:
(一)取样该工业废水,检测其中铬的含量。
步骤Ⅰ: 取25.00 mL废水,加入适量稀硫酸酸化。
步骤Ⅱ:加入过量的碘化钾溶液,Cr2O72-+6I-+14H+![]() 2Cr3++3I2+7H2O然后滴入几滴指示剂。步骤Ⅲ:将一定体积的0.1000mol·L-1 Na2S2O3溶液装入碱式滴定管中,进行滴定操作,滴定结果如下:(I2+2Na2S2O3
2Cr3++3I2+7H2O然后滴入几滴指示剂。步骤Ⅲ:将一定体积的0.1000mol·L-1 Na2S2O3溶液装入碱式滴定管中,进行滴定操作,滴定结果如下:(I2+2Na2S2O3![]() 2NaI+Na2S4O6)
2NaI+Na2S4O6)
滴定次数 | Na2S2O3溶液起始读数/mL | Na2S2O3溶液终点读数/mL |
笫一次 | 1.02 | 19.03 |
第二次 | 2.00 | 19.99 |
第三次 | 0. 20 | 18.20 |
步骤Ⅳ:将上述反应后溶液进行pH调节、过滤等处理,回收沉淀,滤液倒入下水道。
(1)步骤Ⅰ加入稀硫酸酸化的目的是_____________________________;
(2)步驟Ⅱ判断滴定达到终点的现象是___________________________;
(3)以下操作会造成废水中铬含量测定值偏高的是_________________;
A. 滴定终点读数时,俯视滴定管的刻度
B. 盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗
C. 滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
D. 清洗后未用标准液润洗碱式滴定管
(4)25.00mL废水经酸化后,含有Cr2O72- 的物质的量为___________mol.
(二)还原沉淀法除Cr2O72-和CrO42-
该方法的工艺流程为:

(5)能说明第①步反应达到平衡状态的是_____________;(填字母代号)
a. Cr2O72- 和CrO42- 的浓度相同
b. 2v(Cr2O72-)=v(CrO42-)
c. 溶液的颜色不变
(6)第②步中,还原1molCr2O72-离子,需要________mol的FeSO4·7H2O。
(7)常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5 mol·L-1,溶液的pH应调至___________。