题目内容
7.电子数相同的微粒叫做等电子体,下列微粒属于等电子体的是( )| A. | 12CO2和14CO | B. | H2O2和D2O | C. | N2和13CO | D. | NO和CO |
分析 A、12CO2分子含有电子数为20,14CO的电子数为14,
B、H2O2分子含有电子数为18,D2O的电子数为10,
C、N2和13CO的电子数目相同,都是14个电子,
D、NO分子含有电子数为15,CO的电子数为14,
根据题目信息,电子数目相同的微粒为等电子体,据此作判断.
解答 解:A、12CO2分子含有电子数为20,14CO的电子数为14,二者电子数目不相等,不是等电子体,故A错误;
B、H2O2分子含有电子数为18,D2O的电子数为10,二者电子数目不相等,不是等电子体,故B错误;
C、N2和13CO的电子数目相同,都是14个电子,为等电子体,故C正确;
D、NO分子含有电子数为15,CO的电子数为14,二者电子数目不相等,不是等电子体,故D错误;
故选C.
点评 考查等电子体、学生对信息的理解与直接运用,比较基础,有同位素原子的电子计算方法,为该题的易错点.

练习册系列答案
相关题目
17.根据下列短周期元素性质的数据判断,下列说法正确的是( )
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径∕10-10m | 0.66 | 1.36 | 1.23 | 1.10 | 0.99 | 1.54 | 0.70 | 1.24 |
| 最高价或最低价 | -2 | +2 | +1 | +5 -3 | +7 -1 | +1 | +5 -3 | +3 |
| A. | 元素④⑤形成的化合物是离子化合物 | |
| B. | 元素⑦位于第二周期第V族 | |
| C. | 元素①⑧形成的化合物具有两性 | |
| D. | 元素③的最高价氧化物对应水化物的碱性最强 |
18.下列原子的电子排布图中,正确的是( )
| A. | 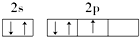 | B. | 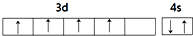 | ||
| C. | 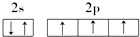 | D. | 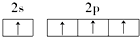 |
15.以下化石能源的加工所得产品不符合事实的是( )
| A. | 石油分馏-乙炔 | B. | 石油裂解-乙烯 | ||
| C. | 煤焦油分馏-苯酚 | D. | 天然气热分解-炭黑 |
19.在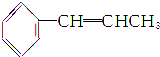 中,处于同一平面内的原子最多有( )
中,处于同一平面内的原子最多有( )
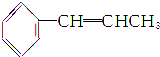 中,处于同一平面内的原子最多有( )
中,处于同一平面内的原子最多有( )| A. | 16个 | B. | 17个 | C. | 18个 | D. | 19个 |
16.在容积一定的密闭容器中,发生可逆反应:A(g)+B(g)?xC(g),有如图(T表示温度,P表示压强,C%表示C的体积分数)所示的反应曲线,则下列说法中正确的是( )
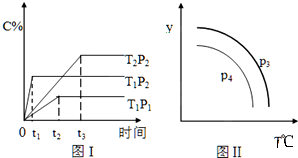

| A. | x=2,T1>T2,P2>P1 | |
| B. | P3>P4,y轴表示B的质量分数 | |
| C. | P3<P4,y轴表示混合气体的密度 | |
| D. | P3>P4,y轴表示混合气体的平均摩尔质量 |
17.下列式子表示的物质一定是纯净物的是( )
| A. | C3H8O | B. | CH2O | C. | C2H4Cl2 | D. | C4H8O2 |
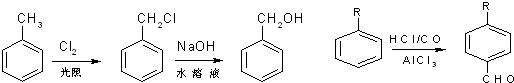
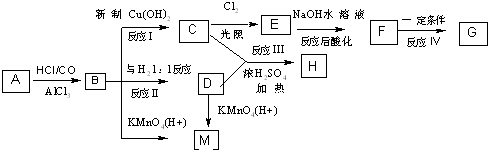
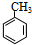 、M
、M ;
; ;C+D→H:
;C+D→H: .
.