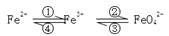题目内容
已知氯化铁溶液跟铜反应生成氯化铜和氯化亚铁。电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)检验溶液中Fe3+存在的试剂是 ,证明Fe3+存在的现象是 。
(2)写出FeCl3溶液与金属铜发生反应的离子方程式(1分):
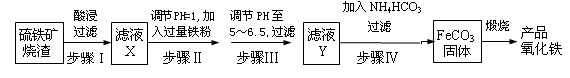
(3)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得FeCl3溶液,准备采用下列步骤:
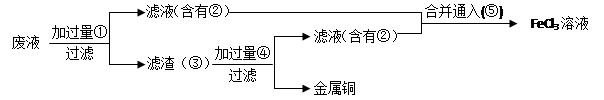
A.请写出上述实验中加入或生成的有关物质的化学式:
① ,② ,④ ,
B.请写出含有②的滤液与⑤反应的离子方程式(1分):
该反应中氧化剂为 还原剂为 。
(1)检验溶液中Fe3+存在的试剂是 ,证明Fe3+存在的现象是 。
(2)写出FeCl3溶液与金属铜发生反应的离子方程式(1分):
(3)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得FeCl3溶液,准备采用下列步骤:

A.请写出上述实验中加入或生成的有关物质的化学式:
① ,② ,④ ,
B.请写出含有②的滤液与⑤反应的离子方程式(1分):
该反应中氧化剂为 还原剂为 。
(9分)(1)KSCN;溶液呈红色 ;(2) 2Fe3++Cu=2Fe2++Cu2+
(3) A.①Fe ,②FeCl2,④HCl B. 2Fe2+ + Cl2 ="=" 2Fe3+ + 2Cl-;Cl2;FeCl2
(3) A.①Fe ,②FeCl2,④HCl B. 2Fe2+ + Cl2 ="=" 2Fe3+ + 2Cl-;Cl2;FeCl2
试题分析:(1)铁离子能和KSCN溶液发生显色反应,溶液显红色,所以检验溶液中Fe3+存在的试剂是能和KSCN溶液。
(2)氯化铁能和氧化金属铜,反应的离子方程式是2Fe3++Cu=2Fe2++Cu2+。
(3)要从废液中回收金属铜,则需要加入还原剂铁粉,即①是Fe。过滤后生成的滤液是氯化亚铁,即②是氯化亚铁。而滤渣中含有铜和剩余的铁,则需要加入稀盐酸溶解铁,即④是HCl。滤液中含有氯化亚铁,要转化为氯化铁,则需要通入氯气将氯化亚铁氧化生成氯化铁即可。
点评:该题是高考中的常见题型,属于中等难度的试题,试题综合性强,注重能力的培养。该类试题,综合性强,理论和实践的联系紧密,有的还提供一些新的信息,这就要求学生必须认真、细致的审题,联系所学过的知识和技能,进行知识的类比、迁移、重组,全面细致的思考才能得出正确的结论。

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案
相关题目