题目内容
【题目】硅是无机非金属材料的主角,硅芯片的使用,促进了信息技术的革命。
![]() 陶瓷、水泥和玻璃都属于传统硅酸盐材料。其中,生产普通玻璃的主要原料除了
陶瓷、水泥和玻璃都属于传统硅酸盐材料。其中,生产普通玻璃的主要原料除了![]() 、
、![]() 外还 ______,玻璃制作过程中发生了
外还 ______,玻璃制作过程中发生了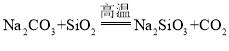 的反应,碳酸酸性强于硅酸,但为什么该反应可在高温下发生? ______。
的反应,碳酸酸性强于硅酸,但为什么该反应可在高温下发生? ______。
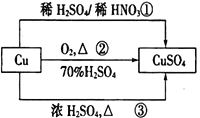
![]() 工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如图:
工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如图:
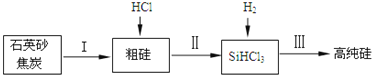
![]() 请写出反应Ⅱ、Ⅲ的化学方程式:Ⅱ ______、Ⅲ ______。
请写出反应Ⅱ、Ⅲ的化学方程式:Ⅱ ______、Ⅲ ______。
![]() 在流化床反应的产物中,
在流化床反应的产物中,![]() 大约占
大约占![]() ,所含有的其它物质的沸点数据如下表:
,所含有的其它物质的沸点数据如下表:
物质 | Si |
|
|
|
| HCl |
|
沸点 | 2355 |
|
|
|
|
|
|
提纯![]() 的主要工艺操作依次是沉降、冷凝和分馏
的主要工艺操作依次是沉降、冷凝和分馏![]() 相当于多次蒸馏
相当于多次蒸馏![]() 。沉降是为了除去 ______ ;在空气中冷凝所得液体主要含有 ______ ;若在实验室进行分馏提纯液体,应该采取以下加热方法中的 ______。
。沉降是为了除去 ______ ;在空气中冷凝所得液体主要含有 ______ ;若在实验室进行分馏提纯液体,应该采取以下加热方法中的 ______。
A.电炉加热![]() 酒精灯加热
酒精灯加热![]() 砂浴加热
砂浴加热![]() 水浴加热
水浴加热
![]() 极易水解,其完全水解时的反应方程式为 ______。
极易水解,其完全水解时的反应方程式为 ______。
【答案】![]() 高温下
高温下![]() 的稳定性比
的稳定性比![]() 强
强 ![]()
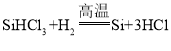 Si
Si ![]() 、
、![]() D
D ![]()
【解析】
![]() 生产普通玻璃的主要原料有:
生产普通玻璃的主要原料有:![]() 、
、![]() 以及
以及![]() ;反应向生成更稳定物质的方向进行;
;反应向生成更稳定物质的方向进行;
![]() 石英砂与焦炭反应得到Si与CO,粗硅与HCl反应得到
石英砂与焦炭反应得到Si与CO,粗硅与HCl反应得到![]() 与氢气,最后再用氢气还原
与氢气,最后再用氢气还原![]() 得到高纯度硅;
得到高纯度硅;
![]() 沉降除去高沸点的硅,在空气中冷凝所得液体的沸点应高于空气的沸点,主要沸点相对较高的
沉降除去高沸点的硅,在空气中冷凝所得液体的沸点应高于空气的沸点,主要沸点相对较高的![]() 、
、![]() ,二者沸点均低于水的沸点,可以利用水浴加热;
,二者沸点均低于水的沸点,可以利用水浴加热;
![]() 极易水解,其完全水解生成原硅酸、氢气与HCl。
极易水解,其完全水解生成原硅酸、氢气与HCl。
![]() 生产普通玻璃的主要原料有:
生产普通玻璃的主要原料有:![]() 、
、![]() 以及
以及![]() ;碳酸酸性强于硅酸,但高温下二氧化硅与碳酸钠反应生成硅酸钠与二氧化碳,说明高温下
;碳酸酸性强于硅酸,但高温下二氧化硅与碳酸钠反应生成硅酸钠与二氧化碳,说明高温下![]() 的稳定性比
的稳定性比![]() 强;
强;
![]() 石英砂与焦炭反应得到Si与CO,粗硅与HCl反应得到
石英砂与焦炭反应得到Si与CO,粗硅与HCl反应得到![]() 与氢气,最后再用氢气还原
与氢气,最后再用氢气还原![]() 得到高纯度硅,反应Ⅱ的化学方程式为:
得到高纯度硅,反应Ⅱ的化学方程式为:![]() ,反应Ⅲ的化学方程式:
,反应Ⅲ的化学方程式: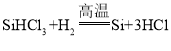 ;
;
![]() 沉降除去高沸点的硅,在空气中冷凝所得液体的沸点应高于空气的沸点,主要沸点相对较高的
沉降除去高沸点的硅,在空气中冷凝所得液体的沸点应高于空气的沸点,主要沸点相对较高的![]() 、
、![]() ,二者沸点均低于水的沸点,可以利用水浴加热(即选项D),受热均匀;
,二者沸点均低于水的沸点,可以利用水浴加热(即选项D),受热均匀;
![]() 极易水解,其完全水解生成原硅酸、氢气与HCl,反应方程式为:
极易水解,其完全水解生成原硅酸、氢气与HCl,反应方程式为:![]() 。
。

 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案【题目】根据下列实验操作和现象所得到的结论正确的是![]()
![]()
选项 | 实验操作 | 实验现象 | 结论 |
A | 向足量含KSCN的 | 溶液变黄 | 还原性:Fe2+>Br- |
B | 向2mL浓度为 | 开始出现白色沉淀,后出现黄色沉淀 |
|
C | 取等质量的Al和Fe,分别与足量的稀硫酸反应 | Al产生的氢气多 | 金属性: |
D | 向苯酚浊液中滴加饱和 | 浊液变澄清 | 酸性:苯酚 |
A.AB.BC.CD.D
【题目】铜及其化合物在工农业生产及日常生活中应用非常广泛.某研究小组用粗铜![]() 含杂质铁
含杂质铁![]() 制备氯化铜晶体
制备氯化铜晶体![]()
![]() 的流程如下:
的流程如下:

已知常温下,![]() 、
、![]() 的氢氧化物开始沉淀和沉淀完全时的pH见下表:
的氢氧化物开始沉淀和沉淀完全时的pH见下表:
金属离子 |
|
|
氢氧化物开始沉淀时的pH |
|
|
氢氧化物完全沉淀时的pH |
|
|
请回答下列问题:
![]() 溶液I中加入试剂X可以调节溶液pH,从而除去
溶液I中加入试剂X可以调节溶液pH,从而除去![]() 且不引入杂质。
且不引入杂质。
![]() 试剂X可选用下列物质中的______
试剂X可选用下列物质中的______![]() 填代号
填代号![]() 。
。
![]()

![]()
![]()
![]() 调节溶液pH时,理论上可选择pH最大范围是______。
调节溶液pH时,理论上可选择pH最大范围是______。
![]() 由溶液Ⅱ制备
由溶液Ⅱ制备![]() 的操作依次为:边滴加浓盐酸边加热浓缩、______
的操作依次为:边滴加浓盐酸边加热浓缩、______![]() 填操作名称
填操作名称![]() 、过滤、洗涤干燥。
、过滤、洗涤干燥。
![]() 室温下,将NaOH溶液逐滴加入到浓度均为
室温下,将NaOH溶液逐滴加入到浓度均为![]() 的
的![]() 和
和![]() 混合溶液中,先生成的沉淀是______
混合溶液中,先生成的沉淀是______![]() 室温时
室温时![]() ,
,![]() 。
。
![]() 某学习小组用碘量法测定
某学习小组用碘量法测定![]() 样品的纯度
样品的纯度![]() 杂质不与发生反应
杂质不与发生反应![]() 实验如下:
实验如下:
![]() 准确称取
准确称取![]() 样品mg于小烧杯中,加入适量蒸馏水和足量的碘化钾,再滴入适量的稀硫酸,充分反应后,将所得混合液配成250mL待测溶液。
样品mg于小烧杯中,加入适量蒸馏水和足量的碘化钾,再滴入适量的稀硫酸,充分反应后,将所得混合液配成250mL待测溶液。![]() 已知:
已知:![]()
![]() 移取
移取![]() 待测溶液于锥形瓶中,加几滴指示剂,用c
待测溶液于锥形瓶中,加几滴指示剂,用c![]() 标准液滴定至终点,重复2次,测得消耗标准液体积的平均值为V
标准液滴定至终点,重复2次,测得消耗标准液体积的平均值为V![]() 。(已知:
。(已知:![]() )
)
![]() 实验中使用的指示剂名称为______,达到滴定终点时的溶液颜色变化为______。
实验中使用的指示剂名称为______,达到滴定终点时的溶液颜色变化为______。
![]() 该样品中
该样品中![]() 的质量分数为______
的质量分数为______![]() 用含m、c、V的代数式表示,不用化简
用含m、c、V的代数式表示,不用化简![]() 。
。
【题目】(1)“84”消毒液是一种常用的消毒剂,其有效成分是______(填化学式)。某学生用石墨作电极电解饱和氯化钠溶液,制作了一种家用环保型消毒液发生器,如图所示。电极c处发生反应的离子方程式依次为:2H2O+2e-=H2↑+2OH-;_____。
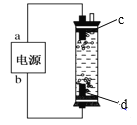
(2)“84”消毒液工业品中常含有1.5%~3%的NaOH,其目的一是使平衡_____(写出离子方程式)向逆方向移动;二是吸收空气中的_____(填化学式)防止消毒液失效。
(3)消毒液中氯元素的存在形态与溶液pH的关系如下:
溶液pH | >9 | 5~6 | 4~5 | 2~3 | <2 |
主要成分 | NaClO | HClO与NaClO(少量) | HClO与Cl2(少量) | HClO与Cl2 | Cl2 |
请你写出pH降低时产生氯气的离子方程式:_____。
(4)某同学猜测“84消毒液”(以下简称“84”)可以“漂白”米醋,进行了实验1和实验2:
编号 | 实验操作 | 实验现象 |
实验1 |
滴加2滴米醋,5滴管“84” | 溶液无色,闻到刺激性气味 |
实验2 |
滴加2滴米醋,5滴管蒸馏水 | 溶液为浅棕色,无刺激性气味 |
实验2的目的是:①______;②______。
为进一步研究“84”与米醋的反应,该同学又进行了以下实验:
编号 | 实验操作 | 实验现象 |
实验3 |
逐滴加入“84”,10滴米醋 | “84”滴入后迅速产生刺激性气味的气体;滴加至5滴时,溶液开始褪色;滴加至21滴时,褪为淡黄色;继续滴加不再出现明显褪色。 |
实验4 |
逐滴加入米醋,21滴“84” | 滴入米醋后立即褪色;当米醋滴加至10滴时,溶液较实验3颜色更浅;当米醋加至17滴时,与实验3中溶液最终颜色相同。 |
请你结合上述实验和相关资料,分析实验3与实验4现象的差异:______。
(5)某工厂使用次氯酸钠漂白棉布,该工厂对生产条件进行了研究,结果如图所示:
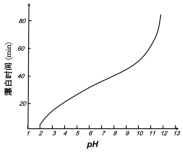
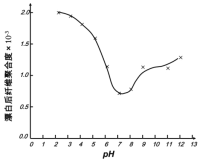
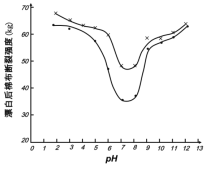
查阅资料得知:次氯酸钠对纤维素的破坏分为两个阶段进行。第一阶段:纤维素纤维的羟基与次氯酸作用生成次氯酸酯;第二阶段:生成的次氯酸酯在OH-离子作用下,失去一分子氯化氢,并转变为醛或酮,直接影响纤维素化学键的稳定性。
①当溶液pH=7时,纤维聚合度最低,纤维损伤最严重的原因是:_____。
②综合考虑,生产过程中pH最好选择_____,理由是_____。