题目内容
5.根据如图,判断下列说法中错误的是( )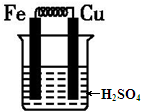
| A. | 铁电极为负极,铜电极为正极 | B. | 导线中电流方向为铁→铜 | ||
| C. | 溶液中阴离子移向铁电极 | D. | 正极电极反应式:2H++2e-═H2↑ |
分析 铁的活泼性大于铜,则铁为负极、铜为正极,负极上铁失去电子生成亚铁离子,正极上氢离子得到电子生成氢气;导线中电流从正极流向负极,即:从铜流向铁;溶液中电流从负极流向正极,阴离子则从正极流向负极,即溶液中阴离子流向铁,据此进行解答.
解答 解:A.铁的活泼性大于铜,所以该原电池中铁为负极、Cu为正极,故A正确;
B.电流从正极流向负极,则导线中电流方向为铜→铁,故B错误;
C.溶液中电流从铁流向铜,则阴离子从铜流向铁,故C正确;
D.正极上氢离子得到电子生成氢气,电极反应式为:2H++2e-═H2↑,故D正确;
故选B.
点评 本题考查了原电池工作原理,题目难度不大,侧重基础知识的考查,明确电解原理即可解答,注意掌握判断电极的方法,能够正确书写电极反应式,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
相关题目
10.下列化合物的化学键中,只有离子键的是( )
| A. | NH4Cl | B. | Na2CO3 | C. | MgCl2 | D. | K2SO4 |
11.设NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4L SO3中原子数目为4NA | |
| B. | 100mL 1mol•L-1的K2CO3溶液中CO32-数目为0.1NA | |
| C. | 5.6g N2与足量H2反应,转移电子数目小于1.2NA | |
| D. | 9.1g苯和立方烷(C8H8)的混合物中原子数目为0.7NA |
20.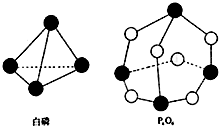 化学反应的本质是旧健的断裂和新键的形成过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ•mol-1)P-P:198 P-O:360 O=O:498,则反应P4(白磷)+3O2→P4O6的能量变化为( )
化学反应的本质是旧健的断裂和新键的形成过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ•mol-1)P-P:198 P-O:360 O=O:498,则反应P4(白磷)+3O2→P4O6的能量变化为( )
 化学反应的本质是旧健的断裂和新键的形成过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ•mol-1)P-P:198 P-O:360 O=O:498,则反应P4(白磷)+3O2→P4O6的能量变化为( )
化学反应的本质是旧健的断裂和新键的形成过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ•mol-1)P-P:198 P-O:360 O=O:498,则反应P4(白磷)+3O2→P4O6的能量变化为( )| A. | 吸收126kJ的能量 | B. | 释放126kJ的能量 | ||
| C. | 吸收1638kJ的能量 | D. | 释放1638kJ的能量 |
17.下列关于有机物的说法中正确的是( )
| A. | 甲烷、一氯甲烷、二氯甲烷等均属于烷烃 | |
| B. | 乙醇不与任何酸反应 | |
| C. | 乙酸不能与金属Na反应 | |
| D. | 乙酸乙酯能发生水解反应 |
14.下列说法中正确的是( )
| A. | 乙醛与新制Cu(OH)2悬浊液反应生成红色的Cu2O沉淀 | |
| B. | 银镜反应中醛发生的是还原反应 | |
| C. | 甲醛、乙醛、丙醛都没有同分异构体 | |
| D. | 醛类催化加氢后都能得到饱和一元醇 |
15.下列变化过程中,只破坏共价键的是( )
| A. | HCl溶于水得盐酸 | B. | NaCl颗粒被粉碎 | ||
| C. | I2升华 | D. | NH4Cl晶体加热分解 |


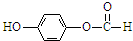 和
和 、
、 (其中两种)
(其中两种)