题目内容
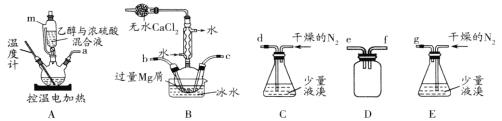
【题目】关于下列装置说法正确的是( )
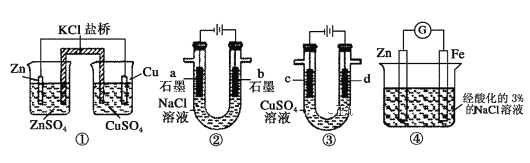
A.装置①中,一段时间后CuSO4浓度增大
B.装置②中滴入酚酞,a极附近变红
C.用装置③精炼铜时,c极为粗铜
D.装置④中发生吸氧腐蚀
【答案】B
【解析】
A. 装置①是原电池,溶液中SO42不参加反应,所以放电过程中硫酸根离子浓度不变,铜电极上,铜离子得到电子变为铜单质,铜离子数量减少,因此CuSO4浓度减小,故A错误;
B. 电解时,b是阳极、a是阴极,阳极上生成氯气、阴极上生成氢气,且阴极附近有NaOH生成,溶液呈碱性,所以a电极附近溶液呈红色,故B正确;
C. 电解精炼粗铜时,粗铜作阳极、纯铜作阴极,所以d为粗铜,故C错误;
D.酸性条件下,锌发生析氢腐蚀,弱酸性或中性条件下,锌发生吸氧腐蚀,该溶液呈强酸性,所以应该发生析氢腐蚀,故D错误;
答案选B。

练习册系列答案
相关题目