题目内容
12.下列物质中,同时含有氯分子、氯离子的是( )| A. | 氯水 | B. | 液氯 | C. | 漂白粉 | D. | 氯化镁 |
分析 同时含有氯分子(Cl2)和氯离子(Cl-),应为混合物,且混合物中含有氯气和氯离子,以此来解答.
解答 解:A.新制氯水中存在Cl2+H2O?HCl+HClO,氯气的溶解度不大,则含氯气、氯离子,故A正确;
B.液氯为单质,只含有氯分子,故B错误;
C.漂白粉的主要成分为氯化钙和次氯酸钙,溶液只含氯离子,不含氯分子,故C错误;
D.氯化镁溶液只含氯离子,不含氯分子,故D错误.
故选A.
点评 本题考查氯水的成分,明确含氯分子的物质中一定含有氯气,明确物质中的成分及物质的电离即可解答,题目难度不大.

练习册系列答案
相关题目
2.用石墨作电极,电解1mol•L-1下列物质的水溶液,溶液的pH保持不变的是( )
| A. | NaOH | B. | HCl | C. | KCl | D. | Na2SO4 |
3.为了降低硫氧化物造成的空气污染,一种方法是在含硫燃料(如煤)燃烧过程中加入生石灰,这种方法叫“钙基固硫”,采用这种方法在燃料燃烧过程中的“固硫”反应为( )
| A. | 2CaO+2S=2CaS+O2↑ | B. | S+O2=SO2 | ||
| C. | CaO+SO2=CaSO3 | D. | 2CaSO3+O2=2CaSO4 |
20.溶液酸碱性探究题
25℃时,某化学兴趣小组在测定酸碱中和滴定曲线的活动中,从实验室领取一瓶一元酸(HA)和一瓶pH=11的碱(BOH)溶液.由于标签破损不知道是何种酸,测得该酸溶液的pH=3.为了进一步认识该酸,请你参与该兴趣小组同学设计实验方案.
(1)证明该一元酸是不是盐酸:
(2)探究HA是强酸还是弱酸:取上述HA和BOH的溶液各20mL混合后溶液的pH=5,试推测HA是强酸还是弱酸.你的结论是弱酸;如果酸是强酸,当体积相等时,pH=3的HA和pH=11的BOH反应只能是中性或碱性,而反应后溶液的pH=5为酸性,所以HA必为弱酸.
(3)若HA是强酸、BOH是强碱,现将此HA溶液和BOH溶液按一定体积比混合后测得溶液的pH=4(设混合后溶液的体积变化忽略不计).则混合时酸和碱的体积之比为V(HA):V(BOH)=11:9.
(4)若HA是强酸,pH=a,BOH是强碱,pH=b,已知a+b=12,两种溶液混合后溶液pH=7,则酸溶液体积V(酸)和碱溶液体积V(碱)的倍数关系是V(碱)100V(酸).
25℃时,某化学兴趣小组在测定酸碱中和滴定曲线的活动中,从实验室领取一瓶一元酸(HA)和一瓶pH=11的碱(BOH)溶液.由于标签破损不知道是何种酸,测得该酸溶液的pH=3.为了进一步认识该酸,请你参与该兴趣小组同学设计实验方案.
(1)证明该一元酸是不是盐酸:
| 滴加试剂 | 所根据的现象 | 结论 |
| 不是盐酸 |
(3)若HA是强酸、BOH是强碱,现将此HA溶液和BOH溶液按一定体积比混合后测得溶液的pH=4(设混合后溶液的体积变化忽略不计).则混合时酸和碱的体积之比为V(HA):V(BOH)=11:9.
(4)若HA是强酸,pH=a,BOH是强碱,pH=b,已知a+b=12,两种溶液混合后溶液pH=7,则酸溶液体积V(酸)和碱溶液体积V(碱)的倍数关系是V(碱)100V(酸).
17.配制相同体积相同物质的量浓度的溶液,所用溶质的质量最大的是( )
| A. | CuCl2 | B. | CaCl2 | C. | K2SO4 | D. | ZnSO4 |
4.下列实验中,①配制一定物质的量浓度的溶液 ②pH试纸的使用 ③过滤 ④蒸发 ⑤溶解,均用到的仪器是( )
| A. | 烧杯 | B. | 漏斗 | C. | 玻璃棒 | D. | 胶头滴管 |
1.由H2、O2、CO2组成的混合气体的密度是同温同压下CH4密度的2倍,三种气体组分的物质的量之比不可能是( )
| A. | 2:3:5 | B. | 2:5:5 | C. | 2:1:5 | D. | 2:2:7 |
4.表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是:Ar(填具体元素符号,下同).
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4,碱性最强的化合物的电子式是: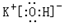 .
.
(3)①~⑨中元素M的最高价氧化物的水化物是两性氢氧化物.则元素M在周期表中的位置是第3周期第ⅢA族(填写具体的周期数和族序数);写出M的氧化物与氢氧化钠溶液反应的化学方程式Al2O3+2NaOH=2NaAlO2+H2O.
(4)用电子式表示元素④与⑥的简单化合物的形成过程: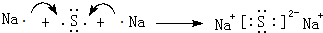 ,该化合物属于离子(填“共价”或“离子”)化合物.
,该化合物属于离子(填“共价”或“离子”)化合物.
(5)由元素②形成的单质的电子式是: ,该物质是由非极性键(填“极性”或“非极性”)键形成的.
,该物质是由非极性键(填“极性”或“非极性”)键形成的.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4,碱性最强的化合物的电子式是:
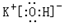 .
.(3)①~⑨中元素M的最高价氧化物的水化物是两性氢氧化物.则元素M在周期表中的位置是第3周期第ⅢA族(填写具体的周期数和族序数);写出M的氧化物与氢氧化钠溶液反应的化学方程式Al2O3+2NaOH=2NaAlO2+H2O.
(4)用电子式表示元素④与⑥的简单化合物的形成过程:
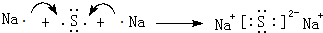 ,该化合物属于离子(填“共价”或“离子”)化合物.
,该化合物属于离子(填“共价”或“离子”)化合物.(5)由元素②形成的单质的电子式是:
 ,该物质是由非极性键(填“极性”或“非极性”)键形成的.
,该物质是由非极性键(填“极性”或“非极性”)键形成的.