题目内容
【题目】酸浸法制取硫酸铜的流程示意图如下

(1)步骤(i)中Cu2(OH) 2CO3 发生反应的化学方程式为______________________。
(2)步骤(ii)所加试剂起调节pH 作用的离子是___________________(填离子符号)。
(3)在步骤(iii)发生的反应中,1 mol MnO2转移2 mol 电子,该反应的离子方程式为______________________。
(4)步骤(iv)除去杂质的化学方程式可表示为:3Fe3++NH4++2SO42-+6H2O=NH4Fe3(SO4)2(OH)6+6H+过滤后母液的pH=2.0,c(Fe3+)=a mol·L-1,c (NH4+)=b mol·L-1,c(SO42-)= d mol·L-1,该反应的平衡常数K=__________(用含a 、b 、d 的代数式表示)。
(5)化学镀的原理是利用化学反应生成金属单质沉积在镀件表面形成镀层。
① 若用CuSO4进行化学镀铜,应选用 ______________(填“氧化剂”或“还原剂”)与之反应。
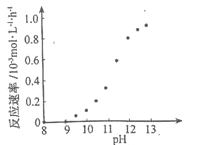
② 某化学镀铜的反应速率随镀液pH 变化如图所示。该镀铜过程中,镀液pH 控制在12.5左右。据图中信息,给出使反应停止的方法:_______________________。
【答案】 Cu2(OH)2CO3 + 2H2SO4 = 2CuSO4 + CO2↑+ 3H2O HCO3- MnO2 + 2Fe2+ + 4H+= Mn2++ 2Fe3+ + 2H2O 10-12/a3bd2 还原剂 调节溶液pH在8~9之间
【解析】(1)碱式碳酸铜与硫酸反应的方程式直接写,用观察法配平.Cu2(OH)2CO3+2H2SO4=2CuSO4+CO2↑+3H2O;
(2)题目要求调高PH,铵根离子显酸性,碳酸氢根离子显碱性,则起作用的离子是碳酸氢根离子;
(3)依题意亚铁离子变成了铁离子,1molMnO2转移电子2mol,则锰元素从+4变成+2价,溶液是显酸性的,方程式经过观察可要补上氢离子,综合上述分析可写出离子方程式为MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;
(4)除去杂质的化学方程式可表示为:3Fe3++NH4++2SO42-+6H2O=NH4Fe3 (SO4)2(OH)6+6H+;过滤后母液的pH=2.0,c(Fe3+)=a molL-1,c( NH4+)=bmolL-1,c( SO42-)=d molL-1,氢离子浓度为10-2,依据K的表达式写出K=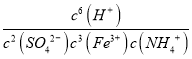 =
=![]() ;
;
(5)①要把铜从铜盐中置换铜出来,比如用铁就可以,铁是作还原剂的,所以加入还原剂;
②根据图示信息,pH=8-9之间,反应速率为0,所以要使反应停止,调节溶液的pH至8-9 之间。

【题目】根据下列实验操作和现象所得出的结论正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 向硅酸钠溶液中滴加盐酸 | 有白色胶状沉淀生成 | 非金属性:Cl>Si |
B | 向溶液X中加入稀盐酸,并将产生的无色无味气体通入澄清石灰水中 | 生成白色沉淀 | 溶液X中一定含有CO32-或HCO3- |
C | 向1mL0.1mol/L MgSO4溶液中,滴入2滴0.1mol/L1NaOH溶液,再滴入2滴0.1mol/LCuSO4溶液 | 起初生成的白色沉淀逐渐变为蓝色沉淀 | Ksp[Cu(OH)2] <Ksp[Mg(OH)2] |
D | 向鸡蛋白溶液中滴入HgCl2溶液 | 有白色沉淀 | 蛋白质发生盐析 |
A. A B. B C. C D. D