题目内容
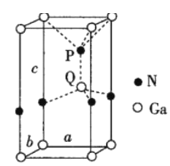
【题目】铅及其化合物用广泛,请回答下列相关问题:
(1)铅是碳的同族元素,比碳多4个电子层。铅元素的原子结构示意图为____________;相同温度下,同浓度的![]() 溶液和
溶液和![]() 溶液中水的电离程度___________(填“前者大”“后者大”或“一样大”)。
溶液中水的电离程度___________(填“前者大”“后者大”或“一样大”)。
(2)工业上利用锌冶炼过程中的铅浮渣(主要成分是![]() 、
、![]() ,含有少量
,含有少量![]() 、
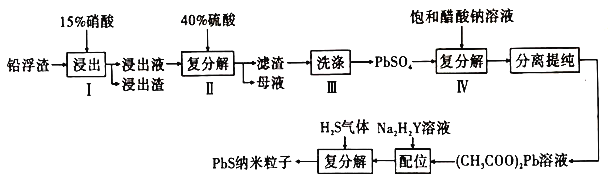
、![]() 和其他不溶于硝酸的杂质)生产硫酸铅和硫化铅纳米粒子,流程如图所示:
和其他不溶于硝酸的杂质)生产硫酸铅和硫化铅纳米粒子,流程如图所示:
已知:a.25℃时,![]() ,
,![]() ,
,![]() 。
。
b.![]() 二钠简写成
二钠简写成![]() ,可以与
,可以与![]() 及其他许多金属离子形成稳定的配离子。
及其他许多金属离子形成稳定的配离子。
①已知步骤Ⅰ有![]() 产生,
产生,![]() 被足量稀硝酸氧化成
被足量稀硝酸氧化成![]() 。写出
。写出![]() 参加反应的离子方程式:________。
参加反应的离子方程式:________。
②步骤Ⅰ需控制硝酸的用量并使![]() 稍有剩余,原因是_________________________。
稍有剩余,原因是_________________________。
③硫酸铅微溶于水,醋酸铅易溶于水,步骤Ⅳ能发生反应的原因是____________________。
④不用硫化氢气体直接通入![]() 溶液来制备
溶液来制备![]() 纳米粒子的原因是__________________。
纳米粒子的原因是__________________。
⑤已知铅蓄电池工作时会产生![]() ,则铅蓄电池
,则铅蓄电池![]() 充电时的阳极反应式为________________________________。
充电时的阳极反应式为________________________________。
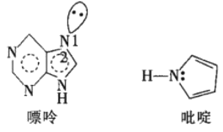
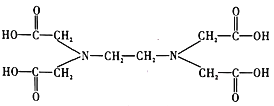
⑥![]() 又名乙二氨四乙酸,是一种弱酸(结构如图),在水溶液中可形成内盐(总电荷为0,电中性的化合物,但是带正电和负电的原子不同)。据此写出
又名乙二氨四乙酸,是一种弱酸(结构如图),在水溶液中可形成内盐(总电荷为0,电中性的化合物,但是带正电和负电的原子不同)。据此写出![]() 的结构:_________________。
的结构:_________________。
【答案】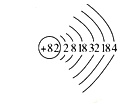 前者大
前者大 ![]() 防止
防止![]() 被溶解进入溶液(或使
被溶解进入溶液(或使![]() 留在浸出渣中)
留在浸出渣中) ![]() 是一种弱电解质,强电解质可以制弱电解质 溶液中
是一种弱电解质,强电解质可以制弱电解质 溶液中![]() 浓度很大,
浓度很大,![]() 很小,直接通
很小,直接通![]() 时,致使
时,致使![]() 的粒子较大,不能形成
的粒子较大,不能形成![]() 纳米粒子
纳米粒子 ![]()
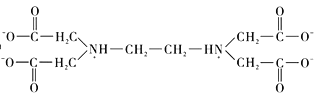
【解析】
(1)既然和碳同族,铅的最外层应该也有4个电子,画出其电子排布即可,水解性盐可以增强水的电离程度,而水解强弱遵循“越弱越水解”的规律;
(2)铅和硝酸发生氧化还原反应,得到![]() ,二氧化铅溶于酸得到
,二氧化铅溶于酸得到![]() ,
,![]() 和铅归中也得到
和铅归中也得到![]() ,硝酸被还原为氮氧化物,加入硫酸得到硫酸铅白色沉淀,后续步骤图中写得比较明确,据此来判断可题即可;
,硝酸被还原为氮氧化物,加入硫酸得到硫酸铅白色沉淀,后续步骤图中写得比较明确,据此来判断可题即可;
(1)根据铅是碳的同族元素,比碳多4个电子层,根据核外电子排布规律,画出铅元素的原子结构示意图为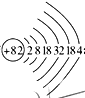 ;根据同族元素性质的递变规律知,非金属性碳强于铅,故
;根据同族元素性质的递变规律知,非金属性碳强于铅,故![]() 酸性强于
酸性强于![]() ,
,![]() 水解程度大于
水解程度大于![]() ,水解促进水的电离,故同浓度的
,水解促进水的电离,故同浓度的![]() 溶液和
溶液和![]() 溶液中水的电离程度前者大;
溶液中水的电离程度前者大;
(2)①![]() 和硝酸的反应类似于铜与稀硝酸的反应,结合提示有
和硝酸的反应类似于铜与稀硝酸的反应,结合提示有![]() 产生,得离子方程式:
产生,得离子方程式:![]() ;
;
②铅浮渣中含有![]() ,
,![]() 也会和硝酸反应,控制硝酸的用量并使
也会和硝酸反应,控制硝酸的用量并使![]() 稍有剩余,可防止
稍有剩余,可防止![]() 被溶解进入溶液(或使
被溶解进入溶液(或使![]() 留在浸出渣中),起到了分离杂质的作用;
留在浸出渣中),起到了分离杂质的作用;
③一般认为绝大多数盐都是强电解质,硫酸铅是强电解质,有极少数盐例外,![]() 就是一个弱电解质,由强电解质制弱电解质自然是可以发生的;
就是一个弱电解质,由强电解质制弱电解质自然是可以发生的;
④![]() 的
的![]() 很小,易沉淀,硝酸铅溶液中
很小,易沉淀,硝酸铅溶液中![]() 浓度很大,直接通
浓度很大,直接通![]() 时,致使
时,致使![]() 的粒子较大,不能形成
的粒子较大,不能形成![]() 纳米粒子,而形成
纳米粒子,而形成![]() 后,游离的
后,游离的![]() 浓度减小;
浓度减小;
⑤铅蓄电池阳极材料为二氧化铅,充电时阳极失电子,由硫酸铅变回二氧化铅,因此电极反应为![]() ;
;
⑥根据两性离子(内盐)的提示,结合氨气与氢离子的反应,可推知![]() 中羧基上的氢可以转移至氮原子上形成内盐,故
中羧基上的氢可以转移至氮原子上形成内盐,故![]() 的结构为
的结构为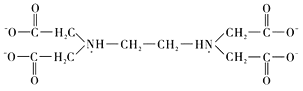 。
。