题目内容
【题目】某同学为了检验浓硫酸与木炭粉在加热条件下反应:[C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O] 产生的所有气体产物,选用了如图所示实验装置。
CO2↑+2SO2↑+2H2O] 产生的所有气体产物,选用了如图所示实验装置。
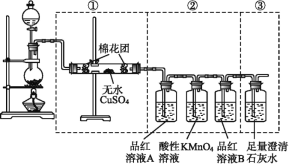
(1)②中酸性KMnO4溶液的作用是____________。
(2)②中两次用到品红溶液,它们的作用分别是A______,B_____。
(3)③中出现的现象是___________。
【答案】吸收SO2 检验SO2 证明SO2被吸收完全 澄清石灰水变浑浊
【解析】
本题的实验目的是检验浓硫酸与木炭粉在加热条件下反应产生的所有气体产物H2O、SO2和CO2。装置图中,第一个加热装置为C和浓硫酸的反应装置,①用来检验水蒸气,②为检验SO2的装置,其中品红溶液A用来检验SO2,酸性KMnO4溶液用来吸收SO2,品红溶液B用来证明SO2被吸收完全,避免后续对CO2的检验产生干扰,③用来检验CO2。
(1)②中酸性KMnO4溶液的作用是吸收SO2;
(2)②中品红溶液A用来检验SO2,品红溶液B用来证明SO2被吸收完全;
(3)③中出现的现象是澄清石灰水变浑浊。

 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案【题目】下列有关物质的制备装置、制备时使用的原料与收集方法均正确的是( )
序号 | 物质 | 制备装置 | 制备时使用的原料 | 收集方法 | 序号 | 物质 | 制备装置 | 制备时使用的原料 | 收集方法 |
A |
|
|
| 排水法 | B | NO |
| 浓硝酸和金属铜 | 排空气法 |
C |
|
| 浓氨水和氢氧化钠固体 | 排空气法 | D |
|
| 乙醇和 | 排水法 |
A.AB.BC.CD.D
【题目】某学生用0.1000 mol/L NaOH溶液滴定未知浓度的盐酸溶液,操作可分解为如下几步:
A.用蒸馏水洗干净滴定管;B. 用待测定的溶液润洗酸式滴定管;C.用酸式滴定管取稀盐酸20.00 mL,注入锥形瓶中,加入酚酞;D.另取锥形瓶,再重复操作一次;E.检查滴定管是否漏水;F.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管“0”刻度以上2~3 cm处,再把碱式滴定管固定好,调节液面至“0”刻度或“0”刻度以下;
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。完成以下填空:
(1)正确操作的顺序是(用序号字母填写)_____________。
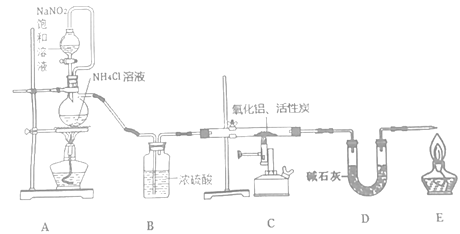
(2)操作F中应该选择图中________滴定管(填标号)。

(3)滴定时边滴边摇动锥形瓶,眼睛应观察________。
A. 滴定管内液面的变化 B. 锥形瓶内溶液颜色的变化
滴定终点溶液颜色的变化是____________________________。
(4)滴定结果如表所示:
滴定次数 | 待测溶液体积/mL | 标准溶液的体积/mL | |
滴定前刻度 | 滴定后刻度 | ||
1 | 20 | 1.02 | 21.03 |
2 | 20 | 2.00 | 25.00 |
3 | 20 | 0.60 | 20.60 |
滴定中误差较大的是第________次实验,造成这种误差的可能原因是________。
A. 碱式滴定管在装液前未用标准NaOH溶液润洗2~3次
B. 滴定开始前碱式滴定管尖嘴部分有气泡,在滴定终点读数时未发现气泡
C. 滴定开始前碱式滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡
D. 达到滴定终点时,仰视溶液凹液面最低点读数
E. 滴定过程中,锥形瓶摇荡得太剧烈,以致有些液滴飞溅出来
(5)该盐酸的浓度为________mol/L。
(6)如果准确移取20.00 mL 0.1000 mol/L NaOH溶液于锥形瓶中,滴入酚酞指示剂,然后用未知浓度的盐酸(装在酸式滴定管中)滴定,是否也可测定出盐酸的物质的量浓度?________(填“是”或“否”)。