��Ŀ����
CO2��CO�ǹ�ҵ�ŷŵĶԻ�������Ӱ��ķ�����
��1����CO2��NH3Ϊԭ�Ϻϳɻ������ص���Ҫ��Ӧ���£�
��2NH3(g)��CO2(g)��NH2CO2NH4(s)����H����159.47 kJ��mol��1
��NH2CO2NH4(s)��CO(NH2)2(s)��H2O(g)����H��a kJ��mol��1
��2NH3(g)��CO2(g)��CO(NH2)2(s)��H2O(g)����H����86.98 kJ��mol��1
��aΪ ��
��2����ѧ��������ù�ҵ�����е�CO2��ȡ�״���CO2+3H2CH3OH+H2O���Ƶõ�CH3OH������ȼ�ϵ�ص�ȼ�ϡ�

����KOH�����У������ĵ缫��ӦʽΪ_________________________________��
�������ʵ�KOH�����õ��K2SO4��Һ�ķ����Ƶá���KOH��_______���ڵõ�,�����ĵ缫��Ӧʽ�ǣ�_____________________________________��
��3������CO��H2��Ӧ�ɺϳ�CH3OCH3��
��֪��3H2(g) + 3CO(g) CH3OCH3(g) + CO2(g)����H��-247kJ/mol
CH3OCH3(g) + CO2(g)����H��-247kJ/mol
��һ�������µ��ܱ������У��÷�Ӧ�ﵽƽ�⣬Ҫ���CO��ת���ʣ����Բ�ȡ�Ĵ�ʩ�� .
��4��CH3OCH3Ҳ����CH3OH�ϳɡ���֪��Ӧ2CH3OH(g)  CH3OCH3(g) + H2O(g)����ij�¶��£���1L�ܱ������м���CH3OH ����Ӧ��10����ʱ�ﵽƽ�⣬��ʱ��ø���ֵ�Ũ�����£�
CH3OCH3(g) + H2O(g)����ij�¶��£���1L�ܱ������м���CH3OH ����Ӧ��10����ʱ�ﵽƽ�⣬��ʱ��ø���ֵ�Ũ�����£�
��0-10 min�ڷ�Ӧ����v(CH3OH) �� ��
�ڸ��¶��µ�ƽ�ⳣ��Ϊ ��
����ƽ��������������ټ���0.01mol CH3OH��0.2mol CH3OCH3����ʱ�����淴Ӧ���ʵĴ�С��
v�� v�� ���>������<������)��
��1����CO2��NH3Ϊԭ�Ϻϳɻ������ص���Ҫ��Ӧ���£�
��2NH3(g)��CO2(g)��NH2CO2NH4(s)����H����159.47 kJ��mol��1
��NH2CO2NH4(s)��CO(NH2)2(s)��H2O(g)����H��a kJ��mol��1
��2NH3(g)��CO2(g)��CO(NH2)2(s)��H2O(g)����H����86.98 kJ��mol��1
��aΪ ��
��2����ѧ��������ù�ҵ�����е�CO2��ȡ�״���CO2+3H2CH3OH+H2O���Ƶõ�CH3OH������ȼ�ϵ�ص�ȼ�ϡ�

����KOH�����У������ĵ缫��ӦʽΪ_________________________________��
�������ʵ�KOH�����õ��K2SO4��Һ�ķ����Ƶá���KOH��_______���ڵõ�,�����ĵ缫��Ӧʽ�ǣ�_____________________________________��
��3������CO��H2��Ӧ�ɺϳ�CH3OCH3��
��֪��3H2(g) + 3CO(g)
 CH3OCH3(g) + CO2(g)����H��-247kJ/mol
CH3OCH3(g) + CO2(g)����H��-247kJ/mol��һ�������µ��ܱ������У��÷�Ӧ�ﵽƽ�⣬Ҫ���CO��ת���ʣ����Բ�ȡ�Ĵ�ʩ�� .
| A�����¸�ѹ�� | B����������� | C�����������뺤���� | D������CO��Ũ�ȣ�E������������� |
 CH3OCH3(g) + H2O(g)����ij�¶��£���1L�ܱ������м���CH3OH ����Ӧ��10����ʱ�ﵽƽ�⣬��ʱ��ø���ֵ�Ũ�����£�
CH3OCH3(g) + H2O(g)����ij�¶��£���1L�ܱ������м���CH3OH ����Ӧ��10����ʱ�ﵽƽ�⣬��ʱ��ø���ֵ�Ũ�����£�| ���� | CH3OH | CH3OCH3 | H2O |
| Ũ��/��mol��L��1�� | 0.01 | 0.2 | 0.2 |
��0-10 min�ڷ�Ӧ����v(CH3OH) �� ��
�ڸ��¶��µ�ƽ�ⳣ��Ϊ ��
����ƽ��������������ټ���0.01mol CH3OH��0.2mol CH3OCH3����ʱ�����淴Ӧ���ʵĴ�С��
v�� v�� ���>������<������)��
��1��+72.49kJ��mol��1 ��2�֣�
��2����CH3OH -6e-+8OH-=CO32-+6H2O��2�֣�
��D ��2�֣�4OH- + 4e- = 2H2O + O2�� ��2�֣�
��3��AE ��2�֣�
��4����0.04 mol��L-1��min-1��2�֣��� 400��2�֣� �� �� ��2��
��2����CH3OH -6e-+8OH-=CO32-+6H2O��2�֣�
��D ��2�֣�4OH- + 4e- = 2H2O + O2�� ��2�֣�
��3��AE ��2�֣�
��4����0.04 mol��L-1��min-1��2�֣��� 400��2�֣� �� �� ��2��
�����������1�������Ȼ�ѧ����ʽ��˹���ɢ�+��=�ۣ��õ�-159.47KJ/mol+a=-86.98KJ/mol��a=+72.49KJ/mol��
��2���ټ״���ȼ���Ƴɵ�ȼ�ϵ�����ɵ�CO2������Һ��������K2CO3���ܷ�ӦʽΪ��2CH3OH+4KOH+3O2=2K2CO3+6H2O,���Լ״��ڸ���ʧȥ���ӣ������ĵ缫��ӦʽΪ��2CH3OH-12e- +16OH- =2CO32- +12H2O��������Ϊ��3O2+12e-+6H2O=12OH-
�ڵ��K2SO4��Һʵ�ʾ��ǵ��ˮ������ˮ�����OH-ʧȥ���ӱ�������������������H+��SO42-ͨ�������ӽ���Ĥ������������A�ڳ��õ����ᣬ�����缫��ӦʽΪ��4OH- + 4e- = 2H2O + O2����������ˮ�����H+�õ����ӱ���ԭ�����Ի��д���OH-���ɣ�K+ͨ�������ӽ���Ĥ������������D�ڳ��õ�KOH��������ӦʽΪ:4H++ 4e- =2H2����
��3���ɷ�Ӧ��֪����ӦΪ���ȡ�ǰ������ϵ�����ٵķ�Ӧ����������ѹǿ�������¶�����������Ӧ���CO��ת���ʣ�����A���У��������ֻ�ܼӿ췴Ӧ���ʣ����ܸı�ƽ�⣬B�����У����������뺤�����ı���μӷ�Ӧ�����Ũ�ȣ�����ı�ƽ�⣬���C������COת���ʣ�����CO��Ũ����ʹƽ�������ƶ�������CO��ת���ʷ������ͣ�E����������������ѣ�����ʹ��Ӧ�����ƶ������������CO��ת���ʣ�����E���У���ѡAE��
��4�����ݱ��������У�2CH3OH(g)
 CH3OCH3(g) + H2O(g)
CH3OCH3(g) + H2O(g)��ʼŨ�ȣ�mol/L���� 0.41 0 0
ת��Ũ�ȣ�mol/L���� 0.4 0.2 0.2
ƽ��Ũ�ȣ�mol/L���� 0.01 0.2 0.2
���Ԣ�0-10 min�ڷ�Ӧ����v(CH3OH) ��0.4 mol/L��10min=0.04 mol��L-1��min-1
�ڸ��¶��µ�ƽ�ⳣ��K=0.2��0.2��0.012 =400
����Ϊ��ƽ��ʱ����������0.01mol CH3OH��0.2mol CH3OCH3 ��0.2mol H2O�������º����������������ټ���ͬ����0.01mol CH3OH��0.2mol CH3OCH3��0.2mol H2O����ﵽ��Чƽ�⣬ƽ�ⲻ�ƶ�������ֻ����0.01mol CH3OH��0.2mol CH3OCH3 ���ܴﵽ��Чƽ�⣬ƽ��������Ӧ�����ƶ������Դ�ʱv��>v�� ��

��ϰ��ϵ�д�
�����Ŀ

 N2(g)+ 2CO2(g)�ġ�H��_______________��
N2(g)+ 2CO2(g)�ġ�H��_______________��
 2NO(g��
2NO(g��  H��0
H��0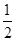 H2(g)+
H2(g)+  2NO2(g) ��H ����ϵ�У�n(NO)��ʱ��ı仯�����
2NO2(g) ��H ����ϵ�У�n(NO)��ʱ��ı仯����� CH3OH(g)��ͼ1��ʾ��Ӧ�е������仯��ͼ2��ʾһ���¶��£������Ϊ1L���ܱ������м���2mol H2��һ������CO��CO��CH3OH(g)��Ũ����ʱ��仯��
CH3OH(g)��ͼ1��ʾ��Ӧ�е������仯��ͼ2��ʾһ���¶��£������Ϊ1L���ܱ������м���2mol H2��һ������CO��CO��CH3OH(g)��Ũ����ʱ��仯��
 CH3OH(g)�Ļ�ѧƽ�ⳣ��Ϊ ���ﵽƽ��������������������䣬���������ѹ��Ϊ0.5L����ƽ�� �ƶ� (�������������)��
CH3OH(g)�Ļ�ѧƽ�ⳣ��Ϊ ���ﵽƽ��������������������䣬���������ѹ��Ϊ0.5L����ƽ�� �ƶ� (�������������)��
 FeO(s) +CO(g) ��H ="a" kJ/mol
FeO(s) +CO(g) ��H ="a" kJ/mol 
 O2(g) �� H2O(g) ��H1
O2(g) �� H2O(g) ��H1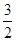 H2(g) �� NH3 (g) ��H3
H2(g) �� NH3 (g) ��H3 O2(g) ��2NO2 (g) ��3H2O(g) �ġ�H��
O2(g) ��2NO2 (g) ��3H2O(g) �ġ�H�� ���ֱ���Ҫ��������436kJ��391KJ��946kJ����N2��H2��Ӧ����1mol NH3(g)���Ȼ�ѧ����ʽ��___________________.
���ֱ���Ҫ��������436kJ��391KJ��946kJ����N2��H2��Ӧ����1mol NH3(g)���Ȼ�ѧ����ʽ��___________________.