题目内容
如图所示,装置在常温下工作(溶液体积变化忽略不计)。闭合K,灯泡发光。下列叙述中不正确的是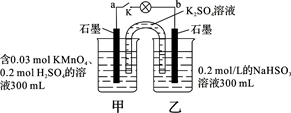
| A.当电路中有1.204×1022个电子转移时,乙烧杯中溶液的pH约为1 |
| B.电池工作时,盐桥中的K+移向甲烧杯,外电路的电子方向是从b到a |
| C.电池工作时,甲烧杯中由水电离出的c(H+)逐渐减小 |
| D.乙池中的氧化产物为SO42- |
C
解析试题分析:闭合K,灯泡发光,说明形成了原电池。A、当电路中有 1.204×1022个电子转移,即有0.02mol的电子转移,乙池发生氧化反应HSO3—2e-+ H2O= SO42-+3 H+,则乙池300mL溶液产生0.03mol H+,H+浓度为0.1mol/L,pH=1,正确;B、乙池是原电池的负极,甲池是原电池的正极,根据原电池中离子的移动方向,则盐桥中的K+移向甲烧杯,外电路的电子方向是从负极流向正极,即由b到a,正确;C、电池工作时,甲烧杯中发生MnO4-+5 e-+8 H+=Mn2++4 H2O,溶液中的氢离子浓度降低,氢氧根离子浓度增大,则由水电离出的c(H+)逐渐增大,错误;D、由A得乙池中的氧化产物为SO42-,正确,答案选C。
考点:考查电化学原理的应用,溶液pH的计算,氧化产物的判断,离子、电子的移动方向的判断

电化学装置工作时,下列电极上发生的反应一定是氧化反应的是( )
| A.阴极 | B.负极 | C.铜电极 | D.石墨电极 |
电解法处理酸性含铬废水(主要含有Cr2O72-)时,以铁板作阴、阳极,处理过程中存在反应Cr2O72+6Fe2++14H+=2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去,下列说法不正确是
| A.阳极反应为Fe-2e- =Fe2+ |
| B.电解过程中溶液pH不会变化 |
| C.过程中有Fe(OH)3沉淀生成 |
| D.电路中每转移12 mol电子,最多有1 mol Cr2O72-被还原 |
锂~碘电池可用来为心脏起搏器提供能源,其电池反应可表示为:2Li + I2 →2LiI。下列有关说法错误的是
| A.放电时化学能转化为电能 | B.负极反应为:Li –e→Li+ |
| C.正极反应为:I2+2e →2I- | D.电子由正极流向负极 |
镍氢电池比碳锌或碱性电池有更大的输出电流,更适合用于高耗电产品。镍氢电池的总反应式是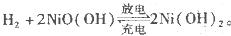 。下列叙述错误的是
。下列叙述错误的是
| A.电池充电时,氢元素被还原 |
| B.电池放电时,镍元素被氧化 |
| C.电池放电时,氢气在负极反应 |
| D.电池放电时,电池负极周围溶液的碱性减弱 |
控制适合的条件,将反应2Fe3++2I- 2Fe2++I2设计成下图所示的原电池。下列判断不正确的是
2Fe2++I2设计成下图所示的原电池。下列判断不正确的是

A.为证明反应的发生,可取甲中溶液加入酸性高锰酸钾溶液 |
B.反应开始时,甲中石墨电极上Fe3+被还原,乙中石墨电极上发生氧化反应 |
C.电流计读数为零时,在甲中加入FeCl2固体后,甲中石墨电极为负极 |
| D.此反应正反应方向若为放热反应,电流计读数为零时,降低温度后,乙中石墨电极为负极 |
某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是
| A.正极反应为AgCl +e-=Ag +Cl- |
| B.放电时,交换膜右侧溶液中有大量白色沉淀生成 |
| C.若用NaCl溶液代替盐酸,则电池总反应随之改变 |
| D.当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子 |
关于下列各图的说法中,正确的是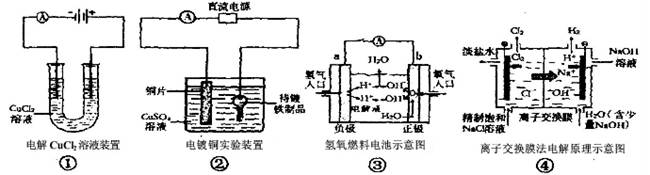
| A.①中与电源负极相连的电极附近能产生使湿润淀粉KI试纸变蓝的气体 |
| B.②中待镀铁制品应该与电源的正极相连接 |
| C.③中的b极是电子流出的极,发生氧化反应 |
| D.④中的离子交换膜可以避免生成的Cl2与NaOH溶液反应 |
 导线
导线