题目内容
某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是
| A.正极反应为AgCl +e-=Ag +Cl- |
| B.放电时,交换膜右侧溶液中有大量白色沉淀生成 |
| C.若用NaCl溶液代替盐酸,则电池总反应随之改变 |
| D.当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子 |
D
解析试题分析:A项正确的正极反应式为Cl2+2e-=2Cl-,错误;B项由于阳离子交换膜只允许阳离子通过,故在左侧溶液中才会有大量白色沉淀生成,错误;C项若用NaCl溶液代替盐酸,但电池总反应不变,错误;D项当电路中转移0.01 mol e-时,交换膜左侧产生0.01 mol Ag+与盐酸反应产生AgCl沉淀,同时约有0.01 mol H+通过阳离子交换膜转移到右侧溶液中,故左侧溶液共约0.02 mol离子减少,正确。
考点:考查原电池知识。

练习册系列答案
相关题目
下图所示原电池工作时,右池中Y2O72-转化为Y3+。下列叙述正确的是
| A.左池电极反应式:X4+ + 2e-=X2+ |
| B.每消耗1mol Y2O72-,转移3mol电子 |
| C.改变右池溶液的c(H+),电流强度不变 |
| D.左池中阴离子数目增加 |
如图所示,装置在常温下工作(溶液体积变化忽略不计)。闭合K,灯泡发光。下列叙述中不正确的是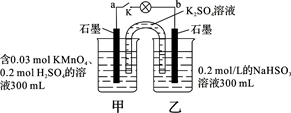
| A.当电路中有1.204×1022个电子转移时,乙烧杯中溶液的pH约为1 |
| B.电池工作时,盐桥中的K+移向甲烧杯,外电路的电子方向是从b到a |
| C.电池工作时,甲烧杯中由水电离出的c(H+)逐渐减小 |
| D.乙池中的氧化产物为SO42- |
如将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2,即构成甲烷燃料电池。已知通入甲烷的一极,其电极反应为CH4+10OH—-8e- CO32—+7H2O,下列叙述正确的是
CO32—+7H2O,下列叙述正确的是
| A.通入甲烷的一极为正极 |
| B.通入氧气的一极发生氧化反应 |
| C.该电池在工作时,溶液中的阴离子向正极移动 |
D.该电池总反应为CH4+2O2+2OH— CO32— +3H2O CO32— +3H2O |
已知:锂离子电池的总反应为:LixC+Li1-xCoO2 C+LiCoO2锂硫电池的总反应为:2Li+S
C+LiCoO2锂硫电池的总反应为:2Li+S Li2S
Li2S
有关上述两种电池说法正确的是
| A.锂离子电池放电时,Li+向负极迁移 |
| B.锂硫电池充电时,锂电极发生还原反应 |
| C.理论上两种电池的比能量相同 |
| D.右图表示用锂离子电池给锂硫电池充电 |
根据下图实验装置判断,下列说法正确的是
| A.该装置能将电能转化为化学能 |
| B.活性炭为正极,其电极反应式为: 2H++2e-=H2↑ |
| C.电子从铝箔流出,经电流表、活性炭、滤纸回到铝箔 |
| D.装置内总反应方程式为:4Al+3O2 +6H2O = 4Al(OH)3 |
下列关于实验现象的描述不正确的是 ( )
| A.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 |
| B.用锌片做阳极,铁片做阴极,电解氯化锌溶液,铁片表面出现一层锌 |
| C.把铜片插入三氯化铁溶液中,在铜片表面出现一层铁 |
| D.把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快 |
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示。下列说法正确的是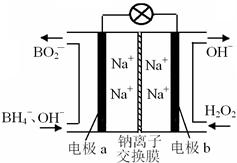
| A.电池放电时Na+从b极区移向a极区 |
| B.电极b采用MnO2,MnO2既作电极材料又有催化作用 |
| C.该电池的负极反应为:BH4-+ 8OH-+8e-→BO2-+ 6H2O |
| D.每消耗3 mol H2O2,转移的电子为3 mol |