题目内容
电解法处理酸性含铬废水(主要含有Cr2O72-)时,以铁板作阴、阳极,处理过程中存在反应Cr2O72+6Fe2++14H+=2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去,下列说法不正确是
| A.阳极反应为Fe-2e- =Fe2+ |
| B.电解过程中溶液pH不会变化 |
| C.过程中有Fe(OH)3沉淀生成 |
| D.电路中每转移12 mol电子,最多有1 mol Cr2O72-被还原 |
B
解析试题分析:A、铁为活泼电极,铁板作阳极时电解过程中电极本身失电子,电极反应式为: Fe-2e-=Fe2+,正确;B、根据题意知,反应过程中溶液中的氢离子浓度减小,溶液pH增大,错误;C、根据Cr2O72+6Fe2++14H+=2Cr3++6Fe3++7H2O知,反应过程中消耗了大量H+,使得Cr3+和Fe3+都转化为氢氧化物沉淀,正确;D、电路中每转移12 mol电子,有6mol Fe2+,结合题给反应知最多有1 mol Cr2O72-被还原,正确。
考点:考查电解原理的应用。

如下图所示,将镁片、铝片平行插入一定浓度的NaOH溶液中,用导线连接成闭合回路,该装置在工作时,下列叙述中正确的是 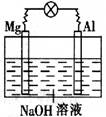
| A.镁比铝活泼,镁失去电子被氧化成Mg2+。 |
| B.铝是电池的负极,开始工作时溶液中会立即有白色沉淀生成 |
| C.该装置的内、外电路中,均是电子的定向移动形成电流 |
| D.该装置开始工作时,铝片表面的氧化膜可不必处理 |
燃料电池是燃料(例如CO,H2,CH4等)跟氧气或空气起反应,将此反应的化学能转变为电能的装置,电解质通常是KOH溶液。下列关于甲烷燃料电池的说法不正确的是
| A.负极反应式为CH4+10OH--8e=CO32-+7H2O |
| B.正极反应式为O2+2H2O+4e=4OH- |
| C.随着不断放电,电解质溶液碱性不变 |
| D.甲烷燃料电池的能量利用率比甲烷燃烧的能量利用率大 |
下图所示原电池工作时,右池中Y2O72-转化为Y3+。下列叙述正确的是
| A.左池电极反应式:X4+ + 2e-=X2+ |
| B.每消耗1mol Y2O72-,转移3mol电子 |
| C.改变右池溶液的c(H+),电流强度不变 |
| D.左池中阴离子数目增加 |
如下图是工业电解饱和食盐水的装置示意图,下列有关说法中不正确的是
| A.装置中出口①处的物质是氯气,出口②处的物质是氢气 |
| B.装置中发生反应的离子方程式为:2Cl-+2H+通电Cl2↑+H2↑ |
| C.该装置是将电能转化为化学能 |
| D.该离子交换膜只能让阳离子通过,不能让阴离子通过 |
用质量均为100g的铜作电极,电解硝酸银溶液(足量),电解一段时间后,两电极的质量差为28g,此时两电极的质量分别为( )
| A.阳极100g,阴极128g | B.阳极93.6g,阴极121.6g |
| C.阳极91.0g,阴极119.0g | D.阳极86.0g,阴极114.0g |
如图所示,装置在常温下工作(溶液体积变化忽略不计)。闭合K,灯泡发光。下列叙述中不正确的是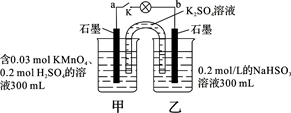
| A.当电路中有1.204×1022个电子转移时,乙烧杯中溶液的pH约为1 |
| B.电池工作时,盐桥中的K+移向甲烧杯,外电路的电子方向是从b到a |
| C.电池工作时,甲烧杯中由水电离出的c(H+)逐渐减小 |
| D.乙池中的氧化产物为SO42- |
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示。下列说法正确的是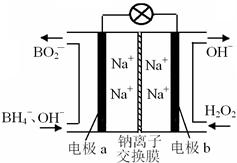
| A.电池放电时Na+从b极区移向a极区 |
| B.电极b采用MnO2,MnO2既作电极材料又有催化作用 |
| C.该电池的负极反应为:BH4-+ 8OH-+8e-→BO2-+ 6H2O |
| D.每消耗3 mol H2O2,转移的电子为3 mol |