题目内容
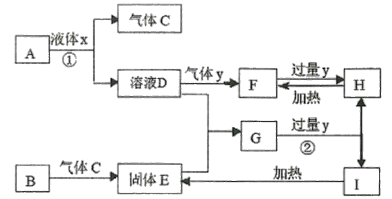
【题目】中学化学常见物质A~I的转化关系如框图所示,其中A为化合物,B为常见金属单质,H的焰色反应为黄色,Y不使品红溶液褪色。(部分反应条件、溶剂及产物已略去)
(1)反应①、②的离子方程式________________、__________。
(2)现有含0.10 mol H的溶液,要使其转化成含0.10 mol F的溶液,则:
①若只能加入0.050 mol的某物质,该物质可能是_________________ (填化学式,写1种)。
②若只能加入0.10 mol的某物质,该物质可能是_________________ (填化学式,写1种)。
【答案】2Na2O2+ 2H2O=4Na++ 4OH- +O2↑ AlO2- + 2H2O +CO2=Al(OH)3↓+ HCO3- Na2O或Na2O2 NaOH或Na
【解析】
由H的焰色反应为黄色,则含有钠元素,且能与F在加热与过量的y之间相互转化,则H为NaHCO3,F为Na2CO3,气体Y为CO2,溶液D为NaOH,化合物A能与液体x反应生成NaOH和气体C,那么A为Na2O2,液体x为H2O;因为B为金属单质,固体E为金属氧化物且能与氢氧化钠反应,则B为Al,E为Al2O3,G为NaAlO2,向NaAlO2通入二氧化碳产生Al(OH)3和NaHCO3,所以I为Al(OH)3,据此回答。
(1)反应①是Na2O2与H2O反应,所以离子反应方程式为2Na2O2+ 2H2O=4Na++ 4OH- +O2↑;反应②是向NaAlO2通入二氧化碳,所以离子反应方程式为:AlO2- + 2H2O +CO2=Al(OH)3↓+ HCO3-;
(2)由分析可知①Na2O或Na2O2,②NaOH或Na。

 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案【题目】某学生探究0.25mol/LAl2(SO4)3溶液与0.5mol/LNa2CO3溶液的反应,实验如下。
实验1 |
|
实验2 |
|
下列分析正确的是( )
A. 实验1中,白色沉淀a是Al2(CO3)3
B. 实验2中,白色沉淀b一定是Al2(OH)2(CO3)2
C. 检验白色沉淀a、b是否洗涤干净,均可用盐酸酸化的BaCl2溶液
D. 实验1、2中,白色沉淀成分不同的原因与混合后溶液的pH无关