��Ŀ����
�����������һ�ֿɴٽ�����������Ӫ�����ʡ���������ƿ�ͨ�����·�Ӧ�Ƶã�
C6H12O6(������)��Br2��H2O��C6H12O7(��������)��2HBr
2C6H12O7(��������)��CaCO3��Ca(C6H11O7)2(���������)��H2O��CO2
������ʵ��ܽ��Լ��±���
| �������� | ��������� | �������� | �廯�� | �Ȼ��� |
| ˮ�е��ܽ��� | ��������ˮ ��������ˮ | ���� | ���� | ���� |
| �Ҵ��е��ܽ��� | �� | �� | ���� | ���� |

��ش��������⣺
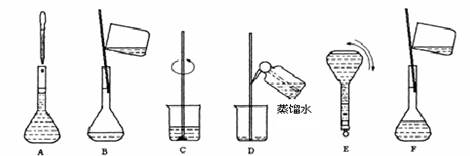
��1���ڢٲ�����ˮ����������ʱ������װ������ʵ���________��
�Ʊ���������ƵĹ����У������ǵ�����Ҳ���������Լ����������������ʺϵ���________��
A������Cu(OH)2����Һ B������KMnO4��Һ
C��O2������������ø D��[Ag(NH3)2]OH��Һ
��2���ڢڲ���ַ�Ӧ��CaCO3��������ʣ�࣬��Ŀ����________����ʵ���в�����CaCl2���CaCO3��������________��
��3���ڢ۲�����ȹ��ˣ���ԭ����________��
��4���ڢܲ������Ҵ���������________��
��5���ڢ��У�����ϴ�Ӽ�����ʵ���________��
A����ˮ B����ˮ C���Ҵ� D���Ҵ���ˮ�����Һ
��1��B��C
��2����������ǵ�ת���ʣ����ں���ķ��룻
��3�������������ȴ���ᾧ���粻���ȹ��˻���ʧ��Ʒ
��4���ɽ����������������Һ�е��ܽ�ȣ���������������Ƶ�����
��5��D
���������������1��������ˮ���÷�Һ©����ˮԡ�����������¶ȡ������ǵ�������O2������������ø������룻A��D��Ҫ���롢�ữ������KMnO4��Һ�������������е�-OH��
���㣺��ѧʵ����������ۡ�

 �Ķ��쳵ϵ�д�
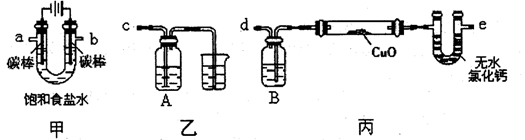
�Ķ��쳵ϵ�д������й�ʵ�������������ʹ����ȷ���� 
A B C D
| A����ȥ�����е��Ȼ��� | B���Ʊ�Fe(OH)2 |
| C��ʵ�����Ʊ����� | D������Ũ���� |
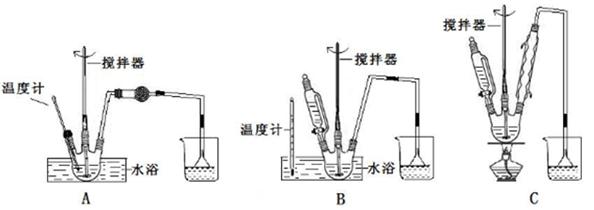
��1��С���������о��¶ȶԷ�Ӧ���ʵ�Ӱ�족ʵ��ʱ����ȡ����ֻ�Թܣ�������4mL 0��01mol/L��KMnO4������Һ��2mL 0��1mol/L H2C2O4���Ҷ��ᣩ��Һ����A�Թ�������ˮ�У�B�Թ�������ˮ�У���¼��Һ��ɫ�����ʱ�䡣
����Ҫ���� ���ữKMnO4��Һ����ɫ����ʱ��tA ��tB�����������=����������
��д���÷�Ӧ�����ӷ���ʽ�� ����
��2��ʵ������ƿ������ɳ���Ҷ�����Ʒ��С�����������Ӧ��ԭ�����ⶨ�京�����������Ϊ��
������250mL��Һ��ȷ����5��0g�Ҷ�����Ʒ�����250mL��Һ��
�ڵζ���ȷ��ȡ25��00mL������Һ����ƿ�У����������ữ����0��1000mol��L��1KMnO4��Һװ��
�� �������ʽ����ʽ�����ζ��ܣ����еζ���������ʵ���з��֣��յ�������KMnO4��Һʱ����ҺѸ�ٱ���Ϻ�ɫ������ƿҡ��һ��ʱ����Ϻ�ɫ������ʧ���ټ����μ�ʱ���Ϻ�ɫ�ͺܿ���ɫ�ˡ������ԭ���� ������ ��֤���ﵽ�ζ��յ㣮
�ۼ��㣺���ظ���������2�Σ���¼ʵ���������£�
| ��� | �ζ�ǰ������mL�� | �ζ��������mL�� |
| 1 | 0��00 | 20��10 |
| 2 | 1��00 | 20��90 |
| 3 | 0��00 | 21��10 |
�������������в����ᵼ�²ⶨ���ƫ�ߵ����� ����
A��δ�ñ�Ũ�ȵ�����KMnO4��Һ��ϴ�ζ���
B���ζ�ǰ��ƿ������ˮ
C���ζ�ǰ�ζ��ܼ��첿�������ݣ��ζ���������ʧ
D����С�Ľ���������KMnO4��Һ������ƿ��
E���۲����ʱ���ζ�ǰ���ӣ��ζ����ӣ�
(15��)������ͭ[Cu(ClO4)2��6H2O]������ˮ��120 �濪ʼ�ֽ⣬�����������缫���������ȡ������Ȼ�ͭͨ�����з�Ӧ�Ʊ���2CuCl2��2Na2CO3��H2O===Cu2(OH)2CO3����CO2����4NaCl��Cu2(OH)2CO3��4HClO4��9H2O===2Cu(ClO4)2��6H2O��CO2����HClO4���ӷ��ķ���Һ�壬�¶ȸ���130 ���ױ�ը���±��г���Ӧ�������������������������pH(��ʼ������pH����������Ũ��Ϊ1 mol��L��1)��
| �������� | ��ʼ���� | ������ȫ |
| Fe3�� | 1��1 | 3��2 |
| Fe2�� | 5��8 | 8��8 |
| Cu2�� | 4��7 | 6��7 |
��1�� ��CuCl2��Na2CO3���в��ֱ���ϸ�����������ķ�ˮ�����裬���ȳ�����ɫ��Һ�����á���ȴ�����ˡ�ϴ�ӵ���ɫCu2(OH)2CO3������
�� �ѷ�Ӧ����ϸ��Ŀ����____________________��
�� ��������Ƿ�ϴ�Ӹɾ���Ӧѡ���Լ���________��
��2�� ��Cu2(OH)2CO3�����еμ��Թ�����HClO4С�Ľ��裬�ʶȼ��Ⱥ�õ���ɫCu(ClO4)2��Һͬʱ����������İ�����
�� �����İ����ijɷ���________(�ѧʽ)��
�� �ʶȼ��ȵ��¶Ȳ��ܹ��ߵ�ԭ����____��
��3�� 25 ��ʱ����������ҺpH��3������Һ�е�Fe3�������ʵ���Ũ��Ϊ________��(��֪25 ��ʱ��Fe(OH)3��Ksp��2��64��10��39)
��4�� ij�о�С�����ô�CuCl2����(��Fe2��)�Ʊ���������ˮ�Ȼ�ͭ���塣�벹�������ɴ�CuCl2�����Ʊ���������ˮ�Ȼ�ͭ�����ʵ�鲽��(��ѡ�õ��Լ�������ˮ��ϡ���ᡢ˫��ˮ��Һ�Ͱ�ˮ)���� ����CuCl2������������ˮ������������ϡ����� ________�����ˣ��� ����Һ________���õ�CuCl2��2H2O���壻�� ��________���õ���ˮ�Ȼ�ͭ���塣