题目内容
1.加成反应(还原反应).(1)写出乙醛与H2反应的方程式;
(2)分析加氢过程中乙醛分子的断键位置.
分析 有机物分子中的不饱和键断裂,断键原子与其他原子或原子团相结合,生成新的化合物的反应是加成反应,一般来说,当有机物中含有C=C、C≡C、C=O键,且反应后转化为C-C、C-O时,发生加成反应,
(1)乙醛分子中含有C=O键能和氢气发生加成生成乙醇;
(2)乙醛分子的结构式为 ,4个碳氢单键、1个碳碳单键、1个碳氧双键,与氢气加成断裂C=O键中的π键.
,4个碳氢单键、1个碳碳单键、1个碳氧双键,与氢气加成断裂C=O键中的π键.
解答 解:(1)乙醛分子中含有C=O键,能与H2反应生成乙醇,反应的方程式为:CH3CHO+H2$→_{△}^{催化剂}$CH3CH2OH,
故答案为:CH3CHO+H2$→_{△}^{催化剂}$CH3CH2OH;
(2)乙醛分子的结构式为 ,和氢气发生加成反应,1个C=O键中含1个σ键和1个π键,π断裂,与氢气加成反应为:
,和氢气发生加成反应,1个C=O键中含1个σ键和1个π键,π断裂,与氢气加成反应为: ++H2$→_{△}^{催化剂}$
++H2$→_{△}^{催化剂}$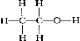 ,
,
故答案为:加氢过程中乙醛分子的断键位置为:乙醛分子结构中C=O键的π断裂.
点评 本题考查了乙醛加成反应的原理,掌握乙醛、乙醇的结构式是解答的关键,题目难度不大.

练习册系列答案
相关题目
9.有一NaOH溶液长期存放在试剂瓶中,结果瓶底溶液呈浑浊状,其原因主要是( )
| A. | 吸收空气中CO2 所致 | |
| B. | NaOH与玻璃作用,而后吸收CO2 所致 | |
| C. | NaOH中含有Na2CO3 | |
| D. | 溶液中的水分部分蒸发 |
16.某链烃0.2mol完全燃烧生成的CO2恰好可被2L 1mol/L NaOH溶液吸收生成正盐,则该烃可能是( )
| A. | 乙烷 | B. | 丙烷 | C. | 正丁烷 | D. | 异戊烷 |
6.有下列反应:
①2Na2SO3 +O2═2Na2SO4(时间不长);
②2H2SO3+O2═2H2SO4(时间较长);
③2SO2 +O2 $\frac{\underline{\;催化剂\;}}{△}$2SO3.
由此说明还原性由弱到强的顺序是( )
①2Na2SO3 +O2═2Na2SO4(时间不长);
②2H2SO3+O2═2H2SO4(时间较长);
③2SO2 +O2 $\frac{\underline{\;催化剂\;}}{△}$2SO3.
由此说明还原性由弱到强的顺序是( )
| A. | Na2SO3、H2SO3、SO3、SO2 | B. | SO2 、H2SO3、Na2SO3 | ||
| C. | H2SO4、SO2 、Na2SO3 | D. | Na2SO3、SO2 、H2SO3 |
13.下列有关实验的选项正确的是( )
| A.配制0.10mol•L-1NaOH溶液 | B.除去CO中的CO2 | C.苯萃取碘水中I2,分出水层后的操作 | D.记录滴定终点读数为12.20mL |
 |  |  | 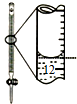 |
| A. | A | B. | B | C. | C | D. | D |
5.向盛有硫酸铜溶液的试管中滴加氨水,首先形成难溶物,继续滴加氨水,难溶物溶解得到深蓝色的透明溶液.下列对此现象说法正确的是( )
| A. | 反应前后Cu2+的浓度不变 | |
| B. | 沉淀溶解后,将生成深蓝色的配离子[Cu(NH3)4]2+ | |
| C. | 向反应后的溶液中加入乙醇,溶液无明显变化 | |
| D. | 在[Cu(NH3)4]2+离子中,Cu2+给出孤对电子,NH3提供空轨道 |
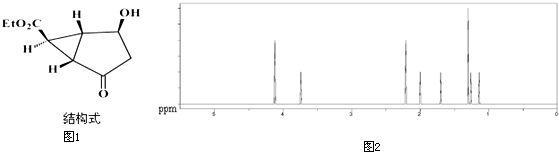
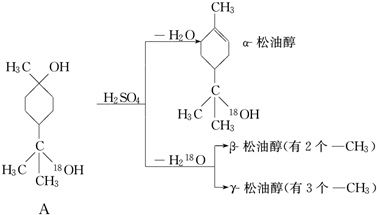
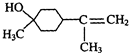 ;γ松油醇:
;γ松油醇: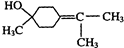 .
.