题目内容
【题目】下表中对应关系错误的是( )
A | NaCl=Na++Cl-; NH3·H2O | 均属于电离方程式 |
B | Ba2++SO HCO | 均可表示一类反应 |
C | SO2使酸性高锰酸钾溶液褪色; SO2使碱性酚酞溶液褪色 | 均利用SO2的同一性质 |
D | Cl2+2NaOH=NaCl+NaClO+H2O; 3S+6NaOH=2Na2S+Na2SO3+3H2O | Cl2和S在反应中既作氧化剂又作还原剂 |
A.AB.BC.CD.D
【答案】C
【解析】
A.氯化钠电离生成钠离子、氯离子,电离方程式为:NaCl=Na++Cl-,一水合氨属于弱电解质,电离生成氨根离子和氢氧根离子,电离方程式为NH3·H2O![]() NH
NH![]() +OH-,A选项正确;
+OH-,A选项正确;
B.Ba2++SO![]() =BaSO4↓可以表示可溶性钡盐与可溶性硫酸盐反应生成硫酸钡沉淀的反应;HCO
=BaSO4↓可以表示可溶性钡盐与可溶性硫酸盐反应生成硫酸钡沉淀的反应;HCO![]() +OH-=CO
+OH-=CO![]() +H2O表示可溶性碳酸氢盐与可溶性强碱反应生成可溶性碳酸盐和水,均可为复分解反应,B选项正确;
+H2O表示可溶性碳酸氢盐与可溶性强碱反应生成可溶性碳酸盐和水,均可为复分解反应,B选项正确;
C.SO2使酸性高锰酸钾溶液褪色体现其还原性;SO2使碱性酚酞溶液褪色体现其酸性氧化物的性质,C选项错误;
D.Cl2+2NaOH=NaClO+H2O+NaCl,反应中氯元素化合价既升高有降低,氯气既作氧化剂又作还原剂,3S+6NaOH=2Na2S+Na2SO3+3H2O,反应中硫元素化合价既升高有降低,硫既作氧化剂又作还原剂,D选项正确;
答案选C。

【题目】I.CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决温室效应的有效途径。
已知反应Fe(s)+CO2(g)![]() FeO(s)+CO(g)的平衡常数为K1;
FeO(s)+CO(g)的平衡常数为K1;
反应Fe(s)+H2O(g)![]() FeO(s)+H2(g)的平衡常数为K2。
FeO(s)+H2(g)的平衡常数为K2。
在不同温度时K1、K2的值如表:
温度 | K1 | K2 |
973K | 1.47 | 2.38 |
1173K | 2.15 | 1.67 |
(1)推导反应CO2(g)+H2(g)![]() CO(g)+H2O(g)的平衡常数K与K1、K2的关系式:___,判断该反应是____反应(填“吸热”或“放热”)。
CO(g)+H2O(g)的平衡常数K与K1、K2的关系式:___,判断该反应是____反应(填“吸热”或“放热”)。
II.T1温度下,体积为2L的恒容密闭容器,加入4.00molX,4.00molY,发生化学反应X(g)+Y(g)![]() 2M(g)+N(s) △H<0。
2M(g)+N(s) △H<0。
部分实验数据如下:
t/s | 0 | 500 | 1000 | 1500 |
n(X)/mol | 4.00 | 2.80 | 2.00 | 2.00 |
(2)前500秒,反应速率v(M)=__ ,该反常数应的平衡K=___。
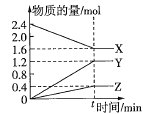
(3)该反应达到平衡时某物理量随温度变化如图所示。纵坐标可以表示的物理量有哪些__。

a.Y的逆反应速率 b.M的体积分数
c.混合气体的密度 d.X的转化率
(4)反应达到平衡后,若再加入2.00molM,1.00molN,下列说法正确的是____。
A.重新达平衡后,用X表示的v(正)比原平衡大
B.重新达平衡后,M的气体体积分数小于50%
C.重新达平衡后,M的物质的量浓度是原平衡的1.25倍
D.重新达平衡后,Y的平均反应速率与原平衡相等
(5)若容器为绝热恒容容器,起始时加入4.00molX,4.00molY,则达平衡后M的物质的量浓度____2mol/L(填“大于”、“小于”或“等于”)。