题目内容
19.下列现象和结论的关系正确的是( )| A. | CO2通入BaCl2溶液中无明显现象,说明碳酸的酸性比盐酸弱 | |
| B. | 氯水加入稀盐酸和AgNO3溶液产生白色沉淀,说明有氯水中有Cl-存在 | |
| C. | 常温下,Cu片投入到浓硫酸中不反应,因为浓硫酸使Cu产生钝化现象 | |
| D. | 浓硫酸具有脱水性,因而能使胆矾失去结晶水由蓝色变白色 |
分析 A.强酸能和弱酸盐反应生成弱酸;
B.稀盐酸中含有氯离子,对氯水中氯离子的检验造成干扰;
C.铜片与浓硫酸在加热条件下反应;
D.浓硫酸具有吸水性,因而能使胆矾失去结晶水由蓝色变白.
解答 解:A.CO2通入BaCl2溶液中无明显现象,则碳酸和盐酸不反应,说明碳酸的酸性比盐酸弱,故A正确;
B.稀盐酸中含有氯离子,对氯水中氯离子的检验造成干扰,故B错误;
C.铜片与浓硫酸在加热条件下反应,不加热不反应,铜与浓硫酸不发生钝化,故C错误;
D.浓硫酸使胆矾失去结晶水由蓝色变白色,体现其吸水性,故D错误;
故选:A.
点评 本题考查了物质的性质,熟悉浓硫酸脱水性与吸水性的区别是解题关键,题目难度不大.

练习册系列答案
相关题目
10.下列物质中,属于纯净物的是( )
| A. | 溴苯 | B. | 铝热剂 | C. | 石油 | D. | 水煤气 |
7.下列关于有机物的说法正确的是( )
| A. | 将甲烷通入溴水中能发生取代反应 | |
| B. | 乙烯双键中的一个键可以断裂,容易发生加成反应 | |
| C. | 乙酸是一种重要的有机酸,是一种无色无味的液体 | |
| D. | 由于乙醇的密度比水小,所以乙醇中的水可以通过分液的方法除去 |
14.下列化学实验的处理及现象不正确的是( )
| A. | 鉴别溶液中是否含有SO42- 时,先滴入稀盐酸使溶液酸化,再滴入氯化钡溶液 | |
| B. | 实验室用H2O2分解制O2,加入少量MnO2后,反应速率明显加快 | |
| C. | 为了加快制取NO气体的速度,可用浓硝酸代替稀硝酸与铜反应 | |
| D. | 检验溶液中是否含有NH4+,可加入足量NaOH溶液,加热,再用湿润的红色石蕊试纸伸入试管内检验是否变蓝 |
4.下列说法正确的是( )
| A. | 原子最外层只有两个电子的元素都在第ⅡA族 | |
| B. | 人们通常在过渡元素中寻找催化剂和耐高温、耐腐蚀的合金材料 | |
| C. | 共价化合物中可能含有离子键 | |
| D. | 水溶液能导电的化合物都是离子化合物 |
11.100mL 6mol•L-1H2SO4跟过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量( )
| A. | 碳酸钠(固体) | B. | 少量硫酸铜溶液 | C. | NaCl溶液 | D. | 加热 |
8.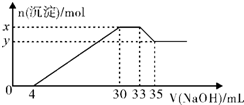 在200mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入5mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示,下列叙述不正确的是( )
在200mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入5mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示,下列叙述不正确的是( )
 在200mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入5mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示,下列叙述不正确的是( )
在200mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入5mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示,下列叙述不正确的是( )| A. | 原溶液中n(Mg2+):n(Al3+)=5:1 | B. | 原溶液的c(H+)=0.1mol•L-1 | ||
| C. | x与y的差值为0.01mol | D. | 原溶液中c(Cl-)=0.85mol•L-1 |
3.25℃时,向10ml0.01mol/LKOH溶液中滴加0.01mol/L苯酚溶液,混合溶液中粒子浓度关系正确的( )
| A. | pH>7时,c(C6H5O-)>c(K+)>c(H+)>c(OH-) | |
| B. | pH<7时,c(K+)>c(C6H5O-)>c(H+)>c(OH-) | |
| C. | V[C6H5OH(aq)]=20ml时,c(C6H5O-)+c(C6H5OH)=2c(K+) | |
| D. | V[C6H5OH(aq)]=10ml时,c(K+)=c(C6H5O-)>c(OH-)=c(H+) |
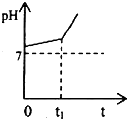 运用化学反应原理研究溶液的组成与性质具有重要意义.请回答下列问题:
运用化学反应原理研究溶液的组成与性质具有重要意义.请回答下列问题: