题目内容
【题目】两种一元碱MOH和ROH的溶液分别加水稀释,溶液pH的变化如图所示,下列叙述正确的是

A. MOH是一种弱碱
B. 在x点,((M+)=c(R+)
C. 稀释前,c(MOH)=l0c(ROH)
D. 稀释前MOH溶液和ROH溶液中由水电离出的c(OH-)前者是后者的10倍
【答案】B
【解析】A、根据图示,溶液稀释100倍,ROH溶液的pH减小了1,MOH溶液pH减小了2,所以MOH是强碱,ROH是弱碱,故A错误;B、在x点,两溶液中pH相等,氢氧根离子浓度等于c(M+)、c(R+),所以c(M+)=c(R+),故B正确;C、由于MOH是强碱,ROH是弱碱,稀释前,MOH等于0.1mol/L,ROH大于0.01mol/L,所以稀释前,c(MOH)<10 c(ROH),故C错误;D、稀释前,MOH溶液中c(OH-)=0.1mol/L,ROH溶液中的c(OH-)=0.01mol/L,由水电离出的c(OH-)分别为10-13 mol/L、10-12 mol/L,因此MOH溶液中水电离的c(OH-)是ROH溶液中由水电离出的氢氧根离子浓度的![]() 倍,故D错误;故选B。
倍,故D错误;故选B。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
【题目】图用分类法表示了一些物质或概念之间的从属或包含关系,不正确的是( )
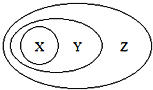
X | Y | Z | |
A | NaAlO2 | 盐 | 纯净物 |
B | 胶体 | 分散系 | 混合物 |
C | Al2O3 | 两性氧化物 | 氧化物 |
D | 单质参与反应 | 置换反应 | 氧化还原反应 |
A. A B. B C. C D. D