题目内容
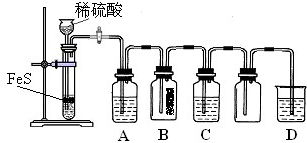
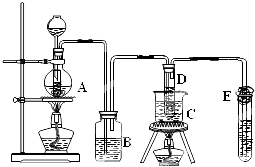 在实验室里制备KClO3,可利用如图所示的装置.实验中的化学原理:
在实验室里制备KClO3,可利用如图所示的装置.实验中的化学原理:①利用强氧化剂和浓盐酸制取氯气;
②使氯气与热的KOH溶液反应制KClO3:3Cl2+6KOH═5KCl+KClO3+3H2O
试回答下列问题:
(1)实验室制备氯气,可选择下列药品中的
A.浓HCl、二氧化锰 B.KMnO4、浓盐酸
C.浓H2SO4、KCl、MnO2 D.浓HNO3、食盐晶体、MnO2
(2)若用MnO2和浓盐酸反应制备氯气,通过上述装置制备KClO3,回答:
①A中发生反应的离子方程式为:
②B中的液体是
③已知C杯中装的是水,D管中装的是15mL 30% KOH溶液,这种加热方式称为
考点:制备实验方案的设计,实验装置综合
专题:实验题
分析:(1)由实验原理可知,强氧化剂与浓盐酸反应制备氯气,只有D中不含浓盐酸;
(2)用MnO2和浓盐酸反应制备氯气,通过上述装置制备KClO3,则A中发生二氧化锰与浓盐酸的反应生成氯气,B为除去氯气中的HCl,C中为水浴加热与KOH反应制备KClO3,便于控制温度,E为尾气处理装置,以此来解答.
(2)用MnO2和浓盐酸反应制备氯气,通过上述装置制备KClO3,则A中发生二氧化锰与浓盐酸的反应生成氯气,B为除去氯气中的HCl,C中为水浴加热与KOH反应制备KClO3,便于控制温度,E为尾气处理装置,以此来解答.
解答:
解:(1)A、MnO2和浓盐酸混合共热、B、KMnO4和浓盐酸均可直接发生氧化还原反应生成氯气,C中KCl和浓硫酸反应生成浓盐酸,再与MnO2共热生成氯气,只有D中不生成浓盐酸,也不能反应生成氯气,故答案为:ABC;
(2)用MnO2和浓盐酸反应制备氯气,通过上述装置制备KClO3,则A中发生二氧化锰与浓盐酸的反应生成氯气,B为除去氯气中的HCl,C中为水浴加热与KOH反应制备KClO3,便于控制温度,E为尾气处理装置,
①A中发生反应的离子方程式为MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O,为防止Cl2从长颈漏斗中逸出,可将长颈漏斗替换成分液漏斗,
故答案为:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O;分液漏斗;
②B中的液体是饱和食盐水,其作用是除去氯气中的HCl气体,故答案为:饱和食盐水;除去氯气中的HCl气体;
③由上述分析可知,加热方式称为水浴加热,其作用是使液体受热均匀,便于控制温度,故答案为:水浴加热;使液体受热均匀,便于控制温度.
(2)用MnO2和浓盐酸反应制备氯气,通过上述装置制备KClO3,则A中发生二氧化锰与浓盐酸的反应生成氯气,B为除去氯气中的HCl,C中为水浴加热与KOH反应制备KClO3,便于控制温度,E为尾气处理装置,
①A中发生反应的离子方程式为MnO2+4H++2Cl-
| ||
故答案为:MnO2+4H++2Cl-
| ||
②B中的液体是饱和食盐水,其作用是除去氯气中的HCl气体,故答案为:饱和食盐水;除去氯气中的HCl气体;
③由上述分析可知,加热方式称为水浴加热,其作用是使液体受热均匀,便于控制温度,故答案为:水浴加热;使液体受热均匀,便于控制温度.
点评:本题考查氯气的制备实验,题目综合性较强,侧重分析能力及实验能力及所学知识分析问题、解决问题的能力的综合考查,难度中等.

练习册系列答案
相关题目
按如图所示装置进行有关实验,则下列叙述正确的是( )
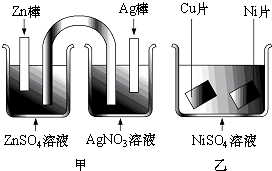

| A、甲装置用作原电池时,锌为正极 |
| B、甲装置用作原电池时,银棒上发生:Ag++e-=Ag |
| C、乙装置用作铜片镀镍时,镍作阴极 |
| D、实现铜片表面镀镍时,可将甲中锌棒与乙中铜片相连,甲中银棒与乙中镍片相连 |
25℃时,在25mL 0.1mol/L NaOH溶液中逐滴加入0.2mol/L HA酸溶液,溶液pH变化曲线如图所示,仔细观察如图,判断有关说法中不正确的是( )
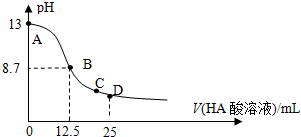

| A、HA酸是弱酸 |
| B、当滴定过程中溶液pH=7时,c(Na+)=c(A-)>c(OH-)=c(H+) |
| C、在C点:c(Na+)>c(A-)>c(H+)>c(OH-) |
| D、在D点:c(A-)+c(HA)=2c(Na+) |
1L的密闭容器中有0.3mol A、0.1mol C和一定量B三种气体.一定条件下发生反应,各物质浓度随时间变化如图甲所示,t1时刻c(B)=0.1mol/L.图乙为t2时刻后改变条件反应速率随时间的变化情况,每次改变一种条件且条件各不相同,已知,t3时刻为加入催化剂,则下列判断正确的是( )
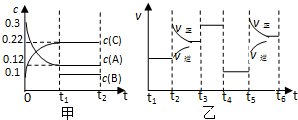

| A、t4时刻是增大容器的体积 |
| B、B的起始浓度为0.06mol/L |
| C、t1、t3、t6时刻相比,A物质的量最大的是t6时刻 |
| D、该可逆反应的方程式为:3A(g)?B(g)+2C(g) |
用NA表示阿伏伽德罗常数.下列说法正确的是( )
| A、标准状况下,11.2L乙烯含有的极性共价键数为NA |
| B、常温下,5.6LNO和5.6LO2的混合气体中含有的分子数为0.5NA |
| C、16.9gBaO2固体中阴、阳离子总数为0.2NA |
| D、含有1molFe(OH)3的氢氧化铁胶体中含有胶粒数为NA |
下列说法不正确的是( )
| A、无热效应的自发过程是不存在的 |
| B、冰融化过程其熵值增加 |
| C、铁生锈、氢气燃烧均为自发放热过程 |
| D、同一物质固态时熵值最小 |
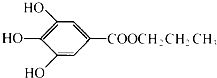 没食子酸丙酯简称PG,是一种白色粉末,难溶于水,微溶于棉子油等油脂,是常用的食用油抗氧化剂.其结构简式如图所示.已知:PG经水解可转化为没食子酸,没食子酸能与NaHCO3溶液反应生成CO2
没食子酸丙酯简称PG,是一种白色粉末,难溶于水,微溶于棉子油等油脂,是常用的食用油抗氧化剂.其结构简式如图所示.已知:PG经水解可转化为没食子酸,没食子酸能与NaHCO3溶液反应生成CO2
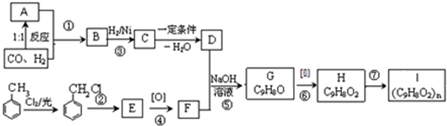
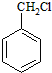 为主要原料合成
为主要原料合成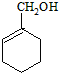 ,请设计四步合成路线(无机试剂及溶剂任选).
,请设计四步合成路线(无机试剂及溶剂任选).