题目内容
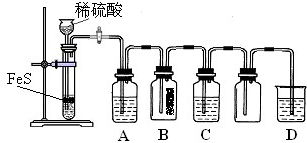
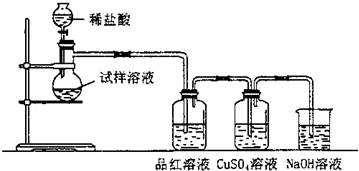
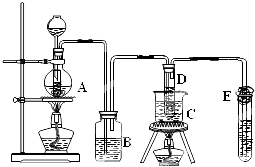
硫化氢(H2S)是一种具有臭鸡蛋气味的无色气体,有剧毒;存在于多种生产过程以及自然界中.在人体的很多生理过程中也起着重要作用.某化学小组设计了制取H2S并验证其性质的实验,如图所示.A中是CuSO4溶液,B中放有湿润的蓝色石蕊试纸,C中是FeCl3溶液.
回答下列问题:
(1)A中有黑色沉淀(CuS)产生,A中发生反应的化学方程式为 .
(2)B中的现象是 .
(3)C中只有浅黄色沉淀产生,且溶液变浅绿色.则C中发生反应的离子方程式为 .
(4)D中盛放的试剂可以是 (填标号).
a.水 b.盐酸 c.NaCl溶液 d.NaOH溶液.

回答下列问题:
(1)A中有黑色沉淀(CuS)产生,A中发生反应的化学方程式为
(2)B中的现象是
(3)C中只有浅黄色沉淀产生,且溶液变浅绿色.则C中发生反应的离子方程式为
(4)D中盛放的试剂可以是
a.水 b.盐酸 c.NaCl溶液 d.NaOH溶液.
考点:制备实验方案的设计,性质实验方案的设计
专题:实验题
分析:由实验装置可知,FeS与稀硫酸反应生成H2S,A中是CuSO4溶液,B中放有湿润的蓝色石蕊试纸,C中是FeCl3溶液,则A中发生CuSO4与H2S反应生成CuS沉淀,B中试纸变红,C中发生氧化还原反应生成S和Fe2+,最后D为尾气处理装置,可利用碱溶液吸收尾气,以此来解答.
解答:
解:(1)CuSO4与H2S反应生成CuS沉淀,反应的方程式为H2S+CuSO4=CuS↓+H2SO4,故答案为:H2S+CuSO4=CuS↓+H2SO4;
(2)H2S水溶液呈酸性,可使湿润的蓝色石蕊试纸变红,故答案为:蓝色石蕊试纸变红;
(3)C中FeCl3具有氧化性,与H2S发生氧化还原反应生成S和Fe2+,反应的离子方程式为H2S+2Fe3+=S↓+2H++2Fe2+,故答案为:H2S+2Fe3+=S↓+2H++2Fe2+;
④H2S有毒,不能排放到空气中,可与碱反应,与水、盐酸、NaCl溶液均不反应,故答案为:d.
(2)H2S水溶液呈酸性,可使湿润的蓝色石蕊试纸变红,故答案为:蓝色石蕊试纸变红;
(3)C中FeCl3具有氧化性,与H2S发生氧化还原反应生成S和Fe2+,反应的离子方程式为H2S+2Fe3+=S↓+2H++2Fe2+,故答案为:H2S+2Fe3+=S↓+2H++2Fe2+;
④H2S有毒,不能排放到空气中,可与碱反应,与水、盐酸、NaCl溶液均不反应,故答案为:d.
点评:本题考查实验制备方案的设计,侧重于硫化氢的性质的设计,题目难度不大,注意把握实验原理和实验的基本操作方法的学习.

练习册系列答案
相关题目
下列物质与盐酸或氢氧化钠溶液反应都能产生气体的是( )
| A、Na2CO3 |
| B、Al(OH)3 |
| C、Al2O3 |
| D、Al |
下列说法中不正确的是( )
| A、相同物质的量的有机物(含C、H、O三种元素中的两种或三种),完全燃烧时,若生成CO2的量与消耗O2的量都相同,则必须符合:不同有机物中碳原子数相同;若分子组成相差n个O原子,则同时相差2n个H原子 |
| B、按系统命名法:CH3CH2C(CH3)2CH(C2H5)CH3的正确名称是3,3,4-三甲基己烷 |
C、1mol的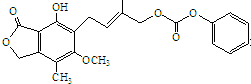 最多能与含6.0mol NaOH的水溶液完全反应 最多能与含6.0mol NaOH的水溶液完全反应 |
D、若完全燃烧,1mol雄酮( )比雌酮( )比雌酮(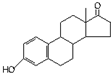 )多消耗3mol O2 )多消耗3mol O2 |
有关如图原电池的说法正确的是( )


| A、盐桥的作用是让电子通过,以构成闭合回路 |
| B、总反应为:2H++Zn═H2+Zn2+且△H<0 |
| C、随着反应进行,右烧杯中溶液pH变小 |
| D、随着反应进行,左烧杯溶液中的SO42-向右烧杯迁移 |

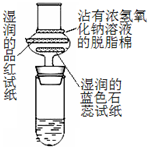 浓硫酸与蔗糖反应的演示实验装置修改如下:实验时在大试管中先放入2g细小颗粒的蔗糖,滴加2-3滴碳酸钠浓溶液,再加入1.5mL 98%的浓硫酸,迅速塞紧带干燥管的单孔橡皮塞.可以看到,蔗糖迅速变黑,体积急剧膨胀,形成多孔海绵状固体物质--“黑面包”.分析实验效果更加明显的原因:
浓硫酸与蔗糖反应的演示实验装置修改如下:实验时在大试管中先放入2g细小颗粒的蔗糖,滴加2-3滴碳酸钠浓溶液,再加入1.5mL 98%的浓硫酸,迅速塞紧带干燥管的单孔橡皮塞.可以看到,蔗糖迅速变黑,体积急剧膨胀,形成多孔海绵状固体物质--“黑面包”.分析实验效果更加明显的原因: ⑥
⑥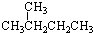 ⑦
⑦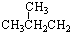 ⑧
⑧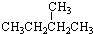
 在实验室里制备KClO3,可利用如图所示的装置.实验中的化学原理:
在实验室里制备KClO3,可利用如图所示的装置.实验中的化学原理: