题目内容
5.在酸性高锰酸钾溶液中加入过氧化钠粉末,溶液褪色,其中发生反应的离子方程式为:2MnO${\;}_{4}^{-}$+16H++5Na2O2═2Mn2++5O2↑+8H2O+10Na+.下列判断正确的是( )| A. | O2是还原产物,Mn2+是氧化产物 | |
| B. | Na2O2既是氧化剂,又是还原剂 | |
| C. | 标准状况下,产生22.4L O2时反应转移2mol e- | |
| D. | 通常用浓盐酸酸化高锰酸钾溶液 |
分析 在2MnO4-+12H++5Na2O2═2Mn2++5O2↑+8H2O+10Na+中,2MnO4-→2Mn2+,Mn元素的化合价由+7价→+2价,得到2×5e-,Mn元素的化合价降低其所在的物质高锰酸钾是氧化剂,5Na2O2→5O2,O元素的化合价由-1价→0价,失去10×e-,过氧化钠是还原剂,以此来解答.
解答 解:A.Mn元素的化合价降低,被还原,O元素的化合价升高被氧化,则O2是氧化产物,Mn2+是还原产物,故A错误;
B.过氧化钠中O元素的化合价升高,则过氧化钠是还原剂,故B错误;
C.标准状况下,产生22.4L O2时反应转移$\frac{22.4L}{22.4L/mol}$×2×[0-(-1)]=2mol e-,故C正确;
D.用浓盐酸酸化高锰酸钾溶液发生氧化还原反应,应利用稀硫酸酸化,故D错误;
故选C.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及转移电子的考查,题目难度不大.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
15.设NA表示阿伏伽德罗常数的数值,下列说法正确的是( )
| A. | 标准状况下,22.4L SO3中含有的分子数为NA个 | |
| B. | 室温下,48.0g氧气和臭氧的混合气体中含有的原子数目为3NA | |
| C. | 过氧化钠与水充分反应生成0.1mol氧气转移的电子数为0.4NA | |
| D. | 0.1mol•L-1的CuCl2溶液中含有0.2NA个Cl- |
16.下列关于自发反应的叙述中,正确的是( )
| A. | 凡是放热反应都是自发的,凡是吸热反应都是非自发的 | |
| B. | 自发反应是无需外界条件就能自发进行的化学反应 | |
| C. | 在通常情况下,冰能自行融化,所以它是自发反应 | |
| D. | 由反应CaCO3(s)=CaO(s)+CO2(g)的特点分析可知其在高温下才能自发进行 |
20.对下面①和②两个结构简式的说法中,正确的是( )
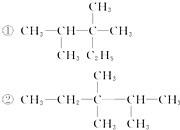

| A. | ①是2,3-二甲基-2-乙基丁烷 ②是3,3,4-三甲基戊烷 | |
| B. | ①②互为同系物 | |
| C. | ①②是同一种物质 | |
| D. | ①②互为同分异构体 |
10.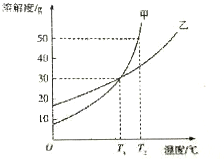 甲、乙两物质的溶解度曲线细图所示,假设溶液的密度为pg•cm-3,溶质的摩尔质量为Mg•mol-1,溶质的物质的量浓度为cmol•L-1,则下列叙述正确的是( )
甲、乙两物质的溶解度曲线细图所示,假设溶液的密度为pg•cm-3,溶质的摩尔质量为Mg•mol-1,溶质的物质的量浓度为cmol•L-1,则下列叙述正确的是( )
 甲、乙两物质的溶解度曲线细图所示,假设溶液的密度为pg•cm-3,溶质的摩尔质量为Mg•mol-1,溶质的物质的量浓度为cmol•L-1,则下列叙述正确的是( )
甲、乙两物质的溶解度曲线细图所示,假设溶液的密度为pg•cm-3,溶质的摩尔质量为Mg•mol-1,溶质的物质的量浓度为cmol•L-1,则下列叙述正确的是( )| A. | T1℃时,甲、乙饱和溶液的物质的量浓度一定相等 | |
| B. | T1℃和T2℃时,甲的饱和溶液的质量分数之比为9:13 | |
| C. | T1℃时,在100g水中加入60g乙,则c(乙)=$\frac{1000×ρ(乙)×37.5%}{M(乙)}$ | |
| D. | T1℃和T2℃时,甲的饱和溶液的物质的量浓度之比为9:13 |
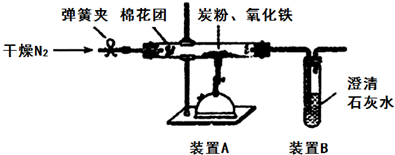
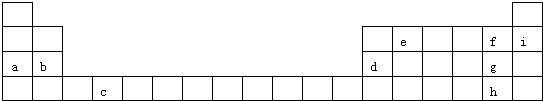
 ;
;