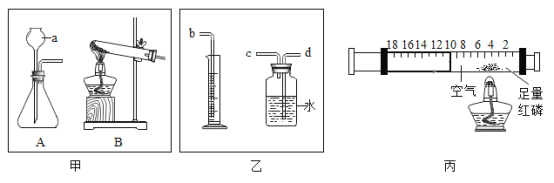
【题目】复方氢氧化镁片[有效成分Mg(OH)2]和复方碳酸镁片[有效成分MgCO3]是两种常见的抗胃酸药。从A或B中任选一个作答,若均作答,按A计分。
A | B |
(1)Mg(OH)2的相对分子质量为___________。 (2)用复方碳酸镁片治疗胃酸过多症时,反应的化学方程式为_____________。 | (1)MgCO3中氧元素质量分数的计算式为___________。 (2)用复方氢氧化镁片治疗胃酸过多症时,反应的化学方程式为__________。 |
【题目】下表是 Na2CO3、NaCl 的溶解度。依据表中数据和实验回答以下小题。
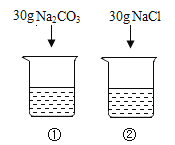
温度 | Na2CO3 | NaCl |
20℃ | 21.8g | 36.0g |
30℃ | 39.7g | 36.3g |
20℃时,向 2 只盛有 100g 水的烧杯中,分别加入 30g 两种固体,充分溶解。
【1】①中溶液的质量为
A.100g
B.121.8g
C.130g
D.139. g 7
【2】上述溶液为饱和溶液的是
A.①
B.①②
C.②
D.无
【3】下列说法正确的是
A.烧杯①中溶质与溶剂的质量比为 3:10
B.烧杯②中溶质的质量分数为 30%
C.烧杯①中溶液升温至 30℃,溶质质量分数不变
D.烧杯①②中溶液升温至 30℃(忽略水的蒸发),溶液质量①=②
【题目】某课外兴趣小组为探究一久置的铝片中铝元素的质量分数,他们取8g该铝片样品放入烧杯中,并依次加入一定质量的相同浓度的稀盐酸,测得相关数据如下,请回答问题。
实验次数 | 1 | 2 | 3 | 4 | 5 |
每次加入稀盐酸的质量/g | 50.0 | 100.0 | 100.0 | 100.0 | 100.0 |
产生气体的总质量/g | 0 | 0.2 | a | 0.6 | 0.7 |
(1)a的数值为_______。
(2)计算所用稀盐酸的溶质质量分数______ (结果保留至0.1%,下同) 。
(3)求该铝片中铝元素的质量分数______。
【题目】某校实验室有一瓶久置的铁粉,已部分锈蚀,某兴趣小组对其组成进行如下探究:
(1)定性探究:
取样品平铺于白纸上,用磁铁置于样品上方,黑色固体全部被吸起,白纸上留下______色固体;将被磁铁吸起的黑色固体全部投入硫酸铜溶液中,充分反应后,过滤,所得固体全部为红色。样品中含有铁和氧化铁。
(2)定量探究:
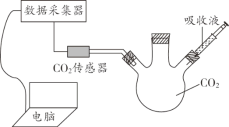
按下图所示装置进行实验(装置气密性良好,固定装置已略去;氮气不与铁屑中的成分反应;碱石灰是氧化钙和氢氧化钠的混合物)。
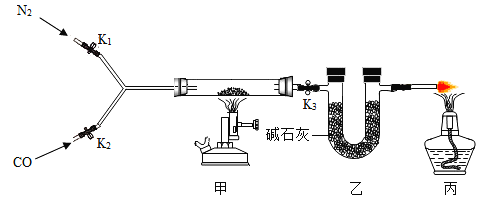
Ⅰ称量硬质玻璃管的质量。将样品放入硬质玻璃管中,称量硬质玻璃管和样品的质量。
Ⅱ连接好装置。缓缓通入N2,燃甲处的酒精喷灯,待硬质玻璃管中固体恒重,记录硬质玻璃管和剩余固体的质量。
Ⅲ再次连接好装置,继续实验。通入CO,点燃丙处的酒精灯和甲处的酒精喷灯。待硬质玻璃管中固体恒重,熄灭酒精喷灯,继续通入CO直至硬质玻璃管冷却。再次记录硬质玻璃管和剩余固体的质量。
数据如下表:
硬质玻璃管 | 硬质玻璃管和样品 | 步骤Ⅱ硬 质玻璃管和剩余固体 | 步骤Ⅲ硬质玻璃管和剩余固体 | |
质量 | m1 | m2 | m3 | m4 |
①步骤Ⅲ丙处酒精灯的作用是_______。
②步骤Ⅲ玻璃管中反应的化学方程式为______。
③样品中氧化铁的质量分数为_______(用m1、m2、m3、m4的代数式表示)。
④若步骤Ⅲ中氧化铁没有完全反应,样品中水的质量分数测量结果将_____(填“偏大”“偏小”或“不变”)。
⑤有关样品,下列说法正确的是_____(填序号,多选)。
A样品中氢元素的质量为![]()
B样品中铁单质和氧化铁的质量总和为m3-m1
C样品中铁单质的质量为m4-m1
D样品中氧元素的质量为m3-m4
【题目】化学兴趣小组的同学发现实验台上一瓶标签破损的无色溶液(标签如下图)。
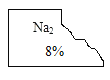
[猜想与假设]
小宁:可能是氢氧化钠溶液;小静:可能是_______溶液;小致:可能是Na2SO4溶液。小远同学认为小宁的猜想不可能,原因是_________。
[实验探究]
实验操作 | 实验现象 | 结论 |
取该溶液少许,滴加_______ | 有气泡产生 | ________同学的猜想成立 |
[反思与评价]标签为什么会破损,小静同学想测定该溶液的酸碱度,她的操作步骤是:________。 测得溶液的pH_______(填“>”“<”或“=”)7,溶液显_______(填“酸”“碱”或“中”)性,倾倒液体时标签未向着手心,致使溶液腐蚀标签,标签破损。