题目内容
【题目】某课外兴趣小组为探究一久置的铝片中铝元素的质量分数,他们取8g该铝片样品放入烧杯中,并依次加入一定质量的相同浓度的稀盐酸,测得相关数据如下,请回答问题。
实验次数 | 1 | 2 | 3 | 4 | 5 |
每次加入稀盐酸的质量/g | 50.0 | 100.0 | 100.0 | 100.0 | 100.0 |
产生气体的总质量/g | 0 | 0.2 | a | 0.6 | 0.7 |
(1)a的数值为_______。
(2)计算所用稀盐酸的溶质质量分数______ (结果保留至0.1%,下同) 。
(3)求该铝片中铝元素的质量分数______。
【答案】0.4 7.3% 90%
【解析】
(1)根据表中数据,第2、3、4次数据分析,每100g稀盐酸完全反应生成氢气质量是0.2g;故a的值为0.4;故填:0.4。
(2)解:设第2次实验所用100.0g稀盐酸中溶质质量为x。

x=7.3g
所用稀盐酸的溶质质量分数为:![]() ×100%=7.3%
×100%=7.3%
答:所用稀盐酸的溶质质量分数为7.3%。
(3)设铝片中铝单质的质量为y。

y=6.3g
氧化铝的质量为:8g-6.3g=1.7g
氧化铝中铝元素的质量为:1.7g×![]() ×100%=0.9g
×100%=0.9g
铝片样品中铝元素质量为:![]() ×100%=90%
×100%=90%
答:该铝片中铝元素的质量分数为90%。

【题目】复方氢氧化镁片[有效成分Mg(OH)2]和复方碳酸镁片[有效成分MgCO3]是两种常见的抗胃酸药。从A或B中任选一个作答,若均作答,按A计分。
A | B |
(1)Mg(OH)2的相对分子质量为___________。 (2)用复方碳酸镁片治疗胃酸过多症时,反应的化学方程式为_____________。 | (1)MgCO3中氧元素质量分数的计算式为___________。 (2)用复方氢氧化镁片治疗胃酸过多症时,反应的化学方程式为__________。 |
【题目】如图所示,在分别盛有100g水的烧杯中放入KNO3充分溶解,则说法正确的是( )
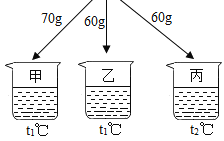
温度(℃) | t1 | t2 |
KNO3的溶解度(g/100g水) | 60 | 90 |
A.甲、乙、丙均为饱和溶液B.乙升温至t2℃,溶液质量增加
C.甲、乙、丙溶液中溶质质量相等D.丙溶液的溶质质量分数是60%