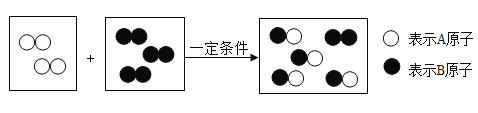
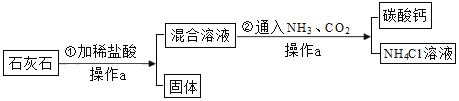
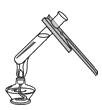
【题目】铜与硫酸在常温下不发生化学反应,在加热条件下是否可以发生化学反应呢?化学学习小组同学开展以下探究活动,请你参与。
(探究活动一)
[实验1] 取某溶质质量分数硫酸溶液于试管中,插入足量的细铜丝加热至沸腾,无明显现象;继续加热一段时间,闻到刺激性气味,溶液显蓝色。
[老师提示]:刺激性气味的气体可能是二氧化硫。
[查阅资料]①二氧化硫可以使品红溶液褪色; ②二氧化硫与二氧化碳部分化学性质相似,能与水反应,也能与氢氧化钠溶液反应。
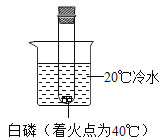
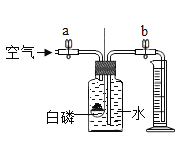
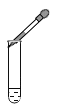
[实验2] 采用如图装置进行实验,验证“实验1” 中产生的气体。(图上硫酸溶液前加上80%)
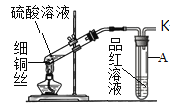
(1)观察到:A试管______________,说明在加热条件下,铜与浓硫酸反应产生了二氧化硫气体。写出该反应的化学方程式:_________________ 。
(探究活动二)
同学们为探究实验1中“加热初始不反应,一段时间后发生反应”的原因,再进行如下实验。
[实验3] 在“实验2”的装置中,把A试管中的品红溶液换成紫色石蕊试液,取几种不同溶质质量分数的硫酸溶液各2mL,分别与质量相同、形状相同的细铜丝进行试验,(每次实验都加热至沸腾的时候),实验结果如下表。
硫酸溶质质量分数 | 98% | 80% | 68% | 44% | 38% | 32% | 20% |
石蕊试液的颜色 | 红色 | 红色 | 红色 | 红色 | 紫色 | 紫色 | 紫色 |
[分析讨论]
(3)上述实验结果表明:在加热至沸腾的条件下,溶质质量分数至少不小于____的硫酸溶液都可以与铜反应。
(4)要获得比实验3的结果即在加热到沸腾时,能与铜反应的硫酸溶液的溶质质量分数更精确的数据范围,请你设计进一步探究的实验方案:_____________ 。
(5)“实验1”中加热至沸腾一段时间后铜才能与硫酸反应的原因是______________。
[反思与评价]
(6)二氧化硫为有毒气体,为防止其污染空气,在“实验2”中,需对实验装置中的导管口K处排出的尾气进行处理,方法是______。
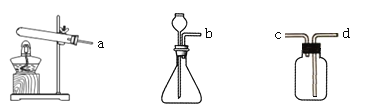
【题目】利用下表所示的实验装置和步骤进行空气中氧气含量的测定[实验前止水夹a、b关闭,容器中的药品(足量)已装入]。下列分析不正确的是
实验装置 | 实验步骤 |
| ①打开a、b,通入空气,当液面下降至某一处,关闭a、b,测得进入量筒中水的体积为V1; ②用强光照射引燃白磷; ③白磷熄灭后冷却至室温,打开b,测得量筒内水的体积为V2。 |
A.步骤①中,液面应下降至燃烧匙以下
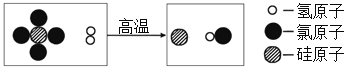
B.白磷燃烧的化学方程式为4P + 5O2![]() 2P2O5
2P2O5
C.步骤③观察到集气瓶中的水流入量筒
D.空气中氧气的体积分数为![]()
【题目】(6分)某校同学开展了如下“溶液酸碱性的检验”的实验活动:

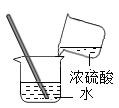
(1)把自制的紫色紫薯汁按图1所示分别滴加到试管中,观察到的现象如下表所示:
溶液 | 白醋 | 盐酸 | 蔗糖水 | 草木灰水 | 石灰水 |
加入紫薯汁后的颜色 | 红色 | 红色 | 紫色 | 绿色 | 绿色 |
①图1中存放紫薯汁的仪器名称 ;
②据上表推测,紫薯汁能做酸碱指示剂,遇到稀硫酸溶液可能显示的颜色是 ;
(2)用PH试纸测定图1中部分溶液的酸碱度:草木灰水pH>7,属于 (填“酸性”“中性”或“碱性”)溶液,白醋pH (填“>””<”或”=”)7;
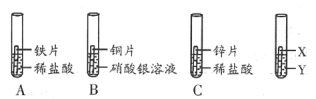
(3)图2是三位同学分别测定土壤酸碱度的操作示意图,其中正确的是 (填“A”“B”或“C”,下同),可能导致北侧溶液pH数值发生改变的错误操作是 。