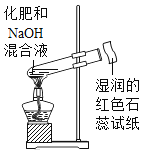
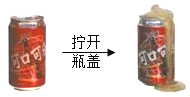
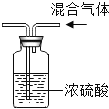
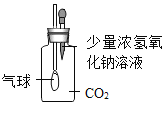
【题目】小晨同学从课外读物中得知:在加热条件下,钠与CO2反应的产物可能有C、CO、Na2CO3、Na2O。于是设计实验对产物成分进行探究。
(查阅资料)①BaCl2溶液呈中性;②4Na+O2=2Na2O;③Na2O+H2O=2NaOH;④2Na+2H2O=2NaOH+H2↑;⑤CO通入PdCl2溶液中有黑色沉淀生成。
(提出问题)在加热条件下,钠与CO2反应的产物有哪些?
(猜想假设)猜想一:产物中一定有C 猜想二:产物中一定有CO
猜想三:产物中一定有Na2CO3 猜想四:产物中一定有Na2O
(实验验证)用下图所示装置(夹持装置已略去)进行实验探究。
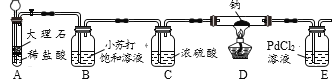
装置A中发生反应的化学方程式为_____;装置C的作用是_____。
序号 | 实验操作 | 实验现象 | 实验结论 |
(1) | 待钠完全反应后,将装置D中的固体置于烧杯中,加蒸馏水溶解 | 有黑色不溶物 | 猜想____正确 |
(2) | 将实验(1)所得混合物过滤,取滤液加入过量BaCl2溶液 | _____ | 猜想三正确 |
(3) | _____ | 猜想二正确 |
(反思与评价)小晨同学向实验(2)所得溶液中滴入几滴酚酞溶液,溶液呈红色。 于是得出结论:在加热条件下,钠与CO2反应一定产生Na2O。该结论是否严谨?____(填“是”或“否”),理由是____。
【题目】实验是学习化学的重要途径,请你根据下列实验装置或仪器,回答问题:
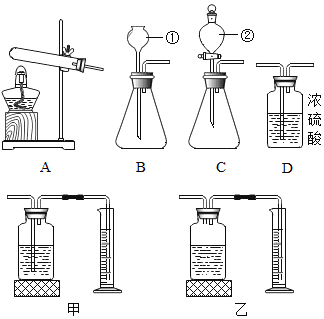
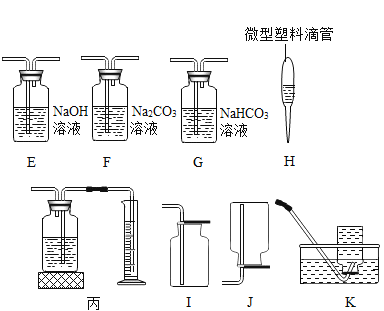
(1)标号①的仪器名称:___________。
(2)请写出实验室用高锰酸钾制取氧气,反应的化学方程式__________,选用K装置收集气体时,下列实验操作正确顺序是______(填序号)。
①反应前,将集气瓶注满水,用玻璃片盖着瓶口,倒立在盛水的水槽中
②开始反应后,等到气泡连续且均匀时,再将导管口移入集气瓶
③收集气体后,将集气瓶盖上玻璃片再移出水槽
实验过程中,发现装置K中的水变为红色,为了防止此现象的发生,改进措施是在A装置中的_________________,为测定一定量的高锰酸钾分解生成氧气的体积,应选用如上述装置______(填编号)。
(3)若取用一定浓度的盐酸与石灰石反应制取气体,将生成的气体缓慢通入澄清石灰水中,未见变浑浊。为探究其原因,进行了如下过程:
(作出猜想)A:石灰水已经完全变质;B:气体中有挥发出来的HCl气体。
(实验探究)①取少量石灰水于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到溶液变红色。于是排除了猜想A,你认为排除猜想A的理由是_______________,上述装置中的数字标号________仪器,也可用H代替。
②为了探究所得气体中是否有挥发出来的HCl气体,设计如下实验。
实验步骤 | 实验现象 | 实验结论 |
将生成的气体通入__________溶液中 | _____________ | 气体中有HCl |
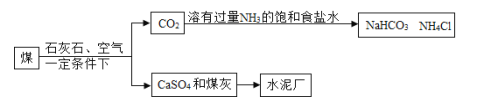
(查阅资料) 碳酸钠溶液中通入二氧化碳发生反应: Na2CO3 + CO2 + H2O = 2NaHCO3
(拓展延伸)如果用上述原料通过控制反应速率制取纯净的二氧化碳气体,所选仪器的连接顺序为____________(填字母)。
【题目】甲、乙、丙、丁四种物质间的反应如图所示,下列选项符合图示反应关系的是:
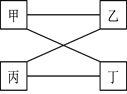
选项 | 甲 | 乙 | 丙 | 丁 |
A | CuO | H2SO4 | CO2 | O2 |
B | Na2SO4 | Ba(OH)2 | HCl | Ba(NO3)2 |
C | NaOH | CO2 | Ca(OH)2 | MgCl2 |
D | Mg | Cu(OH)2 | NaOH | H2SO4 |
A.AB.BC.CD.D