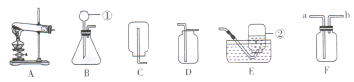
【题目】同学们应用数字化实验探究外界条件对双氧水分解速率的影响.实验装置如图:
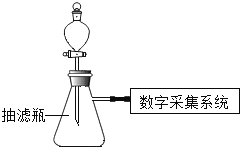
【进行实验】
序号 | 主要实验步骤 | 装置内压强-时间图象 |
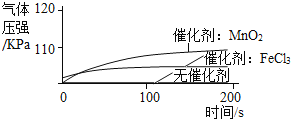
实 验 1 | ①1号抽滤瓶中不加任何试剂, 2号抽滤瓶中加入0.2gMnO2粉末, 3号抽滤瓶中加入0.2gFeCl3粉末. ②用三支分液漏斗分别加入15mL4%的H2O2溶液. |
|
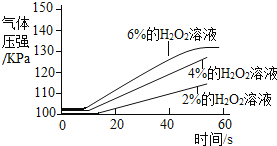
实 验 2 | ①三个抽滤瓶中分别加入0.2gFeCl3粉末. ②分别用1号分液漏斗加入15mL2%的H2O2溶液;用2号分液漏斗加入15mL4%的H2O2溶液;用3号分液漏斗加入15mL6%的H2O2溶液. |
|
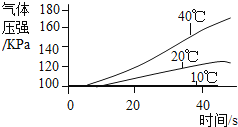
实 验 3 | ①三个抽滤瓶中分别加入0.2gFeCl3粉末,分别放入装有10℃、20℃、40℃水的水槽中. ②用三支分液漏斗分别加入15mL4%的H2O2溶液. |
|
【解释与结论】
(1)实验1的2号抽滤瓶中反应的化学方程式为 ______ .
(2)某同学得到“不同催化剂的催化效果不同”的结论,他的依据是 ______ .
(3)通过上述实验得到:影响该反应速率的外界因素有 ______ .
【反思与评价】
(4)经过多次实验,有的同学对比实验1的3号瓶、实验2的2号瓶中同为40s时的气体压强,发现存在较大的差异,可能的原因是 ______ .
【题目】在学习盐酸的化学性质时,小明和小芳两位同学分别做了碳酸钠溶液和稀盐酸溶液的化学实验(如图).小明的实验中能观察到有气泡产生,小芳的实验中观察不到有气泡产生,对此意外现象,两位同学进行如下探究: 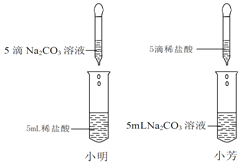
【提出问题】小芳的实验中为什么没有观察到明显现象?
【查阅资料】①碳酸钠和稀盐酸反应不仅可以生成二氧化碳,还可以生成碳酸氢钠.
②碳酸氢钠与氯化钙溶液混合不发生反应;而碳酸钠溶液与氯化钙溶液反应生成沉淀.
【设计实验】证明小芳实验的溶液中含有碳酸氢钠.
实验步骤 | 实验现象 | 实验结论 |
①取上述溶液少量于试管中,加入足量的 ________(写化学式)溶液 | 产生白色沉淀 | 小芳实验的溶液中 含有碳酸氢钠 |
②取步骤①所得上层清液少量,滴加 ______ | _______ |
写出步骤①反应的化学方程式: ______ .
【实验反思】(1)Na2CO3溶液和盐酸溶液反应的生成物受到盐酸量的影响,稀盐酸 ______ (填“过量”或“不足”)时才有气泡冒出.
(2)当反应物的量不同时,产物可能不同,试另举一例: ______ .