题目内容
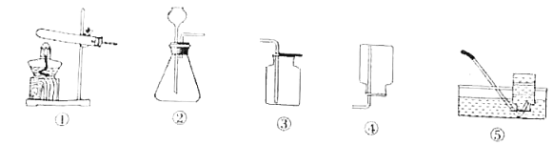
【题目】小明同学用如下图所示的实验装置制取并收集氧气:

(1)请写出有标号仪器的名称:a_______________, b_______________;
(2)若用高锰酸钾制取氧气应选用的发生装置是_______(填序号ABCDEF),反应化学方程式是________,塞棉花的目的是______;要收集较纯净的氧气应选用___________。(填序号ABCDEF)
(3)用氯酸钾和二氧化锰制取氧气的化学方程式___________。
(4)可选择D收集氧气的原因是_____________;
(5)二氧化碳是密度大于空气、可溶于水的气体,实验室用固体石灰石和稀盐酸溶液混合常温制取二氧化碳。则发生装置应选择_________ (填装置编号),收集装置应选_________。 制取二氧化碳的化学方程式______________
【答案】酒精灯 锥形瓶 A 2KMnO4![]() K2MnO4 + MnO2 + O2↑ 防止高锰酸钾粉末进入导管 F 2KClO3
K2MnO4 + MnO2 + O2↑ 防止高锰酸钾粉末进入导管 F 2KClO3![]() 2KCl + 3O2 ↑ 氧气密度比空气大 B或C D CaCO3+2HCl=CaCl2+H2O+CO2↑
2KCl + 3O2 ↑ 氧气密度比空气大 B或C D CaCO3+2HCl=CaCl2+H2O+CO2↑
【解析】
(1)标号a仪器的名称是:酒精灯;标号b仪器的名称是:锥形瓶;
(2)实验室用高锰酸钾制取氧气的反应物是固体,反应条件是加热,所以用高锰酸钾制取氧气应选用的发生装置是A,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4![]() K2MnO4 + MnO2 + O2↑;试管口需要放一团棉花,防止高锰酸钾粉末进入导管,氧气的密度大于空气,不易溶于水,可用向上排空气法或排水法收集。排水法收集的氧气纯净,所以要收集较纯净的氧气应选用F;
K2MnO4 + MnO2 + O2↑;试管口需要放一团棉花,防止高锰酸钾粉末进入导管,氧气的密度大于空气,不易溶于水,可用向上排空气法或排水法收集。排水法收集的氧气纯净,所以要收集较纯净的氧气应选用F;
(3)氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,化学方程式为:2KClO3![]() 2KCl + 3O2 ↑;
2KCl + 3O2 ↑;
(4)D装置收集氧气的方法是向上排空气法,所以可选择D收集氧气的原因是:氧气密度比空气大;
(5)实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,二氧化碳是密度大于空气、可溶于水的气体,所以发生装置应选择B或C,收集装置应选D;石灰石的主要成分是碳酸钙,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑。

 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
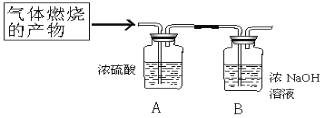
第三学期赢在暑假系列答案【题目】某气体由H2、CO中的一种或两种组成,化学兴趣小组对该气体的组成进行探究。
(提出问题)该气体由什么物质组成?
(提出假设)猜想Ⅰ:只有氢气;猜想Ⅱ:只有一氧化碳;
猜想Ⅲ:________;
(提供信息)由H2、CO中的一种或两种组成的气体能在氧气中安静地燃烧。
(设计实验)将该气体在氧气中完全燃烧的产物依次通过装置A、B,根据装置A、B中物质质量的变化情况来推测该气体的组成。(浓硫酸具有吸水性,NaOH能与二氧化碳反应从而吸收二氧化碳)
(现象与结论)
现象 | 结论 |
①.装置A质量增加, 装置B质量无变化 | 猜想成立______. |
②.装置A质量____,装置B质量增加 | 猜想Ⅱ成立 |
③.装置A质量增加,装置B质量_______. | 猜想Ⅲ成立 |
(分析讨论)
(1)装置A质量增加,说明气体燃烧的产物中有___生成,推知该气体成分中一定含有___元素;装置B质量增加,说明该气体燃烧的产物中有___ 生成,推知该气体成分中一定含有_____元素。
(2)若用石灰水代替浓NaOH溶液,B中能观察到的现象是_________.
(反思)若某纯净物完全燃烧,将其产物依次通过该套实验装置A、装置B,发现装置A、B的质量都增加了,则该纯净物可能是________(任写一种物质的化学式或名称)。