��Ŀ����
����Ŀ��������һ��Զδ��ȫ�����ľ�ѧ��Դ���⣬������Դ���ۺ����þ��зdz�������ǰ������ҵ�ϴӺ�ˮ�п���ȡ����㷺Ӧ��������������Ƽ��ȷ�������ʺ�ԭ�ϡ�
�����Ӻ�ˮ�л�õ�ˮ
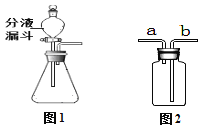
���з��������ں�ˮ��������____________(����ĸ)��
A.���� B.������ C.������ D.���˷�
�Ӻ�ˮ����ȡ��(Br2)
��ҵ��ͨ���ǽ�����ͨ�뺣ˮɹ�κ��ĸҺ�У�����Һ�е��廯��(NaBr)ת��Ϊ�嵥��(Br2)��Ȼ������ȿ�����ʹ�嵥��(Br2)����Һ�лӷ�������������õ����塣�ù�������Ҫ��Ӧ�Ļ�ѧ����ʽΪ_______________________���䷴Ӧ������______________��
�Ӻ�ˮ����ȡ����þ
þ����Ͻ���һ����;�ܹ�Ľ������ϣ���ҵ�ϴӺ�ˮɹ�κ��ĸҺ����ȡþ����Ҫ�������£�
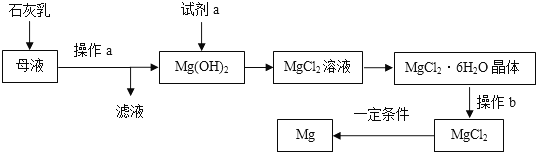
�Իش��������⣺
(1)ʯ������Ҫ�ɷֵĻ�ѧʽΪ_____________��
(2)Mg(OH)2�м����Լ�a������Ӧ�Ļ�ѧ����ʽΪ____________________________��
(3)����b����HCl�����Χ�и������ս��еġ���ֱ������MgCl2��6H2O���壬������MgO���������ֻ����д���йط�Ӧ�Ļ�ѧ����ʽ___________________________ ��
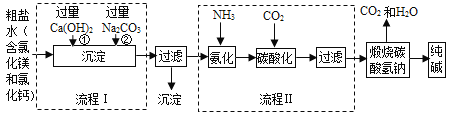
�����Ժ�ˮ����ȡ��ʳ��Ϊԭ���Ʊ�����
�Ʊ���������Ҫ�漰����������Ӧ��
�� CO2+NH3+H2O �T�TNH4HCO3
�� NH4HCO3 + NaCl�T�TNaHCO3 �� + NH4Cl
�� 2NaHCO3 ![]() Na2CO3+ CO2 �� + H2O
Na2CO3+ CO2 �� + H2O
�Իش��������⣺
(1)�Ʊ������п���ֱ��ѭ���������õ�������H2O��__________________��
(2)��ʵ������֤����Ӧ���е�NaHCO3����ȫ�ֽ�ľ��������________��
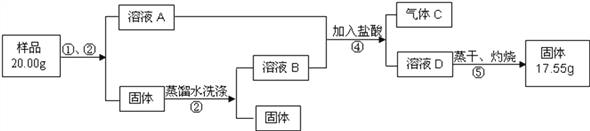
(3)ij��ѧ��ȤС����Ϊ����̼��������ȫ�ֽ������£����õĴ�����Ҳ��������Է�Ӧ���е����ʣ�Ϊ�����ǽ���������̽����
a��ȡ2.2g������Ʒ����ˮ��ȫ�ܽ��100g��Һ��
b������100g 3.65%��ϡ���
c��ȡ����һ����Һ25g����ƿ�У��ٽ���һ����Һ��μ�����ƿ�ڣ���Ӧ����Һ��pH�仯�������ͼ��ʾ��
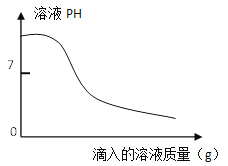
����c�е�������һ����ҺΪ10gʱ����ƿ������ǡ����ȫ��Ӧ������Ʒ��̼���Ƶ���������Ϊ___________(д��������̣�����������1λС��)
���𰸡� A Cl2 + NaBr �T�T NaCl + Br2 �û���Ӧ Ca(OH)2 2HCl+ Mg(OH)2�T�T MgCl2+ 2H2O MgCl2��6H2O![]() MgO + 2HCl��+5H2O�� CO2 ȡ�ֽ�����Ʒ�������������м������գ����ֹ��������������仯��˵���ֽ���ȫ��(��ȡ�ֽ�����Ʒ�����Թ��м��ȣ�û�в�����ʹ����ʯ��ˮ����ǵ����壬˵���ֽ���ȫ) 96.4 %
MgO + 2HCl��+5H2O�� CO2 ȡ�ֽ�����Ʒ�������������м������գ����ֹ��������������仯��˵���ֽ���ȫ��(��ȡ�ֽ�����Ʒ�����Թ��м��ȣ�û�в�����ʹ����ʯ��ˮ����ǵ����壬˵���ֽ���ȫ) 96.4 %
�����������������dz�ȥҺ���еĹ��岻�����һ�ַ�������ķ���������Ҳ�Ƿ�����岻������Һ�������һ�ַ����������dz�ȥҺ���е�ɫ�ء���ζ���ʵ�һ�ַ�������ķ��������������ַ���ֻ�ܳ�ȥ���ܵĹ��岻�ܵ�����ˮ���������ܳ�ȥ�����Ե����ʣ��ʿ��Ե�����ˮ��ȥ��ˮ�п����Ե�ʳ����
���������廯�Ʒ�Ӧ�����Ȼ��ƺ��壬��ѧ����ʽΪ��Cl2 + NaBr�T NaCl + Br2����Ӧ��һ�ֵ��ʺ�һ�ֻ����ﷴӦ������һ�ֵ��ʺ���һ�ֻ�����Ļ�ѧ��Ӧ�������û���Ӧ��
������1��ʯ������Ҫ�ɷ����������ƣ���ѧʽΪCa(OH)2��
��2��Mg(OH)2�м����Լ�a������Ӧ�������Ȼ�þ������aΪHCl���Ļ�ѧ����ʽΪ��2HCl+ Mg(OH)2�T MgCl2+ 2H2O��
��3������MgCl2��6H2O���壬������MgO��ˮ���Ȼ��⣬��ѧ����ʽΪ��MgCl2��6H2O ![]() MgO + 2HCl��+5H2O����
MgO + 2HCl��+5H2O����
������1���ɷ���ʽ��֪���Ʊ������п���ֱ��ѭ���������õ�������H2O��CO2��
��2��̼���������ȷֽ�Ϊ̼���ơ�ˮ�Ͷ�����̼������ȡ�ֽ�����Ʒ�������������м������գ����ֹ��������������仯��˵���ֽ���ȫ����ȡ�ֽ�����Ʒ�����Թ��м��ȣ�û�в�����ʹ����ʯ��ˮ����ǵ����壬˵���ֽ���ȫ��
��3��������֪���뵽��ƿ����ҺΪϡ����
�μӷ�ӦHCl��������10g��3.65% =0.365g
�⣺��μӷ�Ӧ̼���Ƶ�����ΪX
Na2CO3+2HCl�T2NaCl + H2O + CO2��
106 73
X 0.365g
![]()
X=0.53g
̼���Ƶ�������0.53g��![]() =2.12g
=2.12g
̼���Ƶ�����������![]() ��100% ��96.4 %
��100% ��96.4 %
�𣺴�����Ʒ��̼���Ƶ���������Ϊ96.4 %��