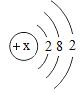
题目内容
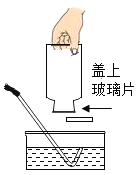
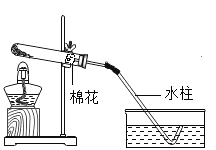
【题目】下图是验证CO2性质的实验装置。实验时,持续通入CO2。
步骤Ⅰ:打开K1,关闭K2,观察现象。
步骤Ⅱ:关闭K1,打开K2,加热c,一段时间后,观察现象。
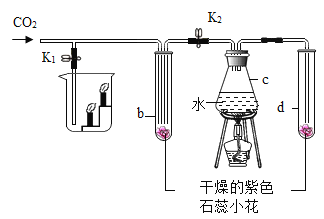
(1)步骤Ⅰ烧杯中蜡烛熄灭的原因是_____。
(2)上述实验过程中,能证明CO2与水反应的实验现象是_____。
【答案】不支持燃烧的二氧化碳进入烧杯,隔绝了氧气 步骤Ⅰb中小花不变红,步骤Ⅱb中小花变红,d中小花不变红
【解析】
(1)不支持燃烧的二氧化碳通过导管通到烧杯的底部,将密度比二氧化碳小的空气排出烧杯外,使蜡烛与空气中的氧气隔离,蜡烛的燃烧停止,故填隔绝了氧气。
(2)步骤Ⅰ中打开K1,关闭K2,b中的干燥的紫色石蕊小花只与二氧化碳接触,小花不变红,步骤Ⅱ加热c,水受热成为水蒸气,水蒸气沿导管进入b、d,b中的干燥的受热小花遇到水和二氧化碳,水与二氧化碳反应生成碳酸,碳酸使受热变红,d中的干燥的紫色受热小花只与水接触,没有二氧化碳,小花不变红,即证明CO2与水反应的实验现象是步骤Ⅰb中小花不变红,步骤Ⅱb中小花变红,d中小花不变红,故填步骤Ⅰb中小花不变红,步骤Ⅱb中小花变红,d中小花不变红。

 阅读快车系列答案
阅读快车系列答案【题目】甲、乙、丙、丁四种物质的相互反应关系如图所示(“一” 表示相连的物质间能发生反应)下列符合对应反应关系的选项是
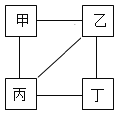
选项 | A | B | C | D | |
物质 | 甲 | BaCl2 | CO2 | H2 | Fe |
乙 | Na2CO3 | NaOH | O2 | HCI | |
丙 | H2SO4 | CaCl2 | CuO | CuSO4 | |
丁 | Ca(OH)2 | AgNO3 | CO | NaOH | |
A.AB.BC.CD.D
【题目】某实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解,进行了如下实验:
(一)制取氧化铜
①称取2 g 胆矾,研细后倒入烧杯,加10 mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不再产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀全部变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用。
(1)上述实验步骤中需要使用玻璃棒的有____(选填实验序号);步骤①、③中研磨固体所用仪器的名称是_____。
(2)步骤③中洗涤沉淀的操作是_____。
(二)证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较
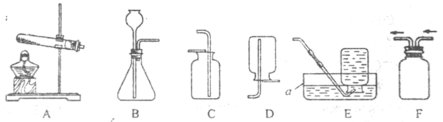
用如图装置进行实验,实验时均以生成25 mL气体为准,其它可能影响实验的因素均已忽略,相关数据见下表:
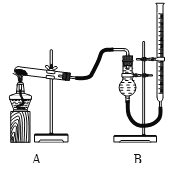
实验序号 | KClO3质量 | 其它物质质量 | 待测数据 |
④ | 1.2 g | 无其他物质 | |
⑤ | 1.2 g | CuO 0.5 g | |
⑥ | 1.2 g | MnO2 0.5 g |
(3)上述实验中的“待测数据”指___。
(4)若要证明实验⑤中干燥管内收集的气体是O2,可待气体收集结束后,用弹簧夹夹住A、B之间的乳胶管,拔去干燥管上单孔橡皮塞,______。
(5)为探究CuO在实验⑤中是否起催化作用,还需补做如下两项实验:
a ____(描述操作过程及目的);
b证明CuO的化学性质有没有改变。