题目内容
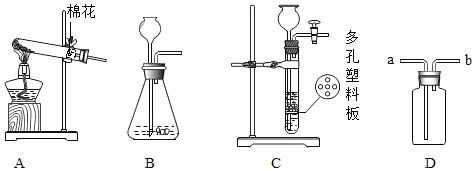
【题目】如图,A,B分别是某微粒的结构示意图,请回答下列问题.
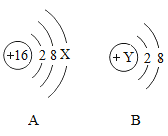
(1)A表示的是硫原子的结构示意图,则X=________,该元素在化学反应中易________(填“失去”或“得到”)电子形成离子;
(2)若B是某种带两个单位正电荷的阳离子的结构示意图,则Y=________.
【答案】6 得到 12
【解析】
(1)根据当核电荷数=质子数=核外电子数,为原子,故A表示的是硫原子的结构示意图,则X=16﹣8﹣2=6;最外层电子数大于等于4的在化学反应中易得到电子形成阴离子;故该元素的原子在化学反应中容易得到电子;
(2)在离子中,阳离子所带电荷数=核内质子数﹣核外电子数,所以若B是某种带两个单位正电荷的阳离子的结构示意图,则Y=2+8+2=12;
答案:(1)6;得到; (2)12.

 黄冈创优卷系列答案
黄冈创优卷系列答案【题目】某同学在做“氢气在空气中燃烧”实验时,对生成物的成分产生了质疑:水和过氧化氢具有相同的组成元素,那么氢气在空气中燃烧除生成水外,是否还有过氧化氢生成呢?带着疑问,该同学利用如图所示实验装置进行了以下探究。
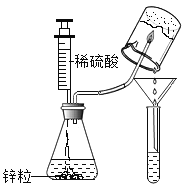
(提出猜想)氢气在空气中燃烧除生成水,还有过氧化氢生成。
(查阅资料)
①在一定条件下(低温环境下),氢气在空气中燃烧除生成水外,还有过氧化氢生成。
②过氧化氢溶液能使无色的淀粉碘化钾溶液变蓝色。
③低温时过氧化氢难分解
(实验探究)
主要步骤 | 主要现象 | 实验结论 |
Ⅰ.将注射器内的稀硫酸注入到盛有锌粒的锥形瓶中 | 在锌粒表面有______产生 | 反应的化学方程式为___________ |
Ⅱ.点燃经验纯后的氢气,用底部结有冰的小烧杯罩在火焰上方,用漏斗和试管收集所得液体。向试管中加入______。 | 氢气燃烧产生淡蓝色火焰,试管中液体由无色变_____色 | 氢气在空气中燃烧有过氧化氢生成 |
(反思评价)实验中将氢气燃烧的火焰对着冰,冰的作用是______。
A创设低温环境,使部分氢气燃烧产生一定量的过氧化氢
B使生成的过氧化氢溶入冰融化成的水中,便于收集
C有利于防止生成的过氧化氢分解
(拓展分析)除氢气和氧气反应会生成两种氧化物外,金属钠也具有类似的化学性质。钠常温露置在空气中与氧气反应生成氧化钠,钠在空气中燃烧生成过氧化钠(Na2O2);造成反应物相同,生成物不同的原因是________。
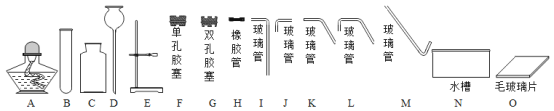
【题目】某CO气体中混有少量的CO2,为探究CO的性质,某同学在老师的指导下设计了以下实验装置,请填写下列空白.
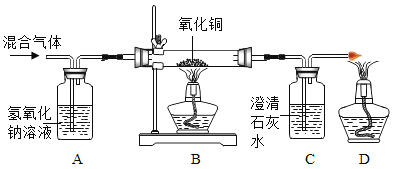
(1)A装置的作用是___________.B处玻璃管内的现象是___________.
(2)C处反应的化学方程式为___________;
(3)实验时,应___________(选填“先”或“后”)点燃B处的酒精灯;
(4)某同学对B处玻璃管内剩余固体成分产生浓厚兴趣.
(提出问题)B处玻璃管内的剩余固体是什么?
(假设猜想)猜想①:剩余固体全部是铜 猜想②:剩余固体是铜和氧化铜的混合物
(实验设计)
实验步骤 | 实验中可能出现的现象 | 结论 |
取B处玻璃管内少量剩余固体于试管中加入 ___________ | 现象一:固体不溶解,溶液不变色 | 猜想①___________(选填“成立”或“不成立”) |
现象二: ___________ | 猜想②成立 |
(拓展延伸)
(Ⅰ)D处酒精灯的作用是___________;
(Ⅱ)根据B处的反应原理,CO可用于___________.
【题目】某公司生产的新型融雪剂,其成分是无水CaCl2和少量的NaCl,为测定CaCl2的含量,同学称取该样品12g,加水充分溶解成溶液,然后取一定质量分数的Na2CO3溶液分五次加入,充分振荡,实验数据见表。取你分析数据并进行诱导计算。
次数 | 1 | 2 | 3 | 4 | 5 |
加入Na2CO3溶液的质量/g | 20 | 20 | 20 | 20 | 20 |
生成沉淀的质量/g | 2.5 | x | 7.5 | 10 | 10 |
(1)上表x=_________。
(2)样品中CaCl2的质量分数________。