题目内容
【题目】化学学科的特征是在原子、分子水平上研究物质和创造物质.
(1)请从微观的角度解释:金属Na、Mg性质不同的原因是_____;CO和CO2性质不同的原因是_____;HCl、H2SO4可以使紫色石蕊试剂变红的原因是_____.
(2)A、B、C、D四种物质的微观示意图如图1表示:
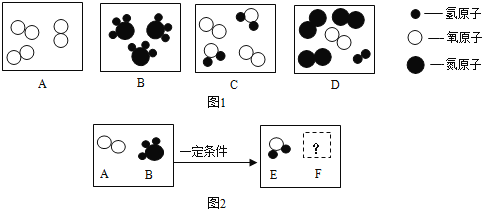
(ⅰ)从微观角度看,B图表示:_____(填化学符号);
(ⅱ)从宏观角度看,图中表示混合物的是_____(填字母编号);
(3)在一定条件下,A和B能发生化学反应生成E和F,其微观示意图如图2所示:
(ⅰ)若F为空气中体积分数最大的气体,写出该反应的化学方程式_____.
(ⅱ)一定条件下,若反应中A、B和E的分子个数比为5:4:6,则F的化学式为_____.
【答案】原子的最外层电子数不同 分子的构成不同 溶液中都含有氢离子 NH3 CD 3O2+4NH3 6H2O+2N2 NO
6H2O+2N2 NO
【解析】
(1)物质的结构决定物质的性质,金属Na、Mg性质不同的原因是原子的最外层电子数不同;CO和CO2性质不同的原因是分子的构成不同;HCl、H2SO4可以使紫色石蕊试剂变红的原因是溶液中都含有氢离子;
(2)(ⅰ)从微观角度看,B图表示的分子是由一个氮原子和三个氢原子构成的;
(ⅱ)从宏观角度看,图中CD物质是由不同种物质组成的,属于混合物;
(3)①F是氮气时其反应物是氧气与氨气,产物是水与氮气,其方程式是:3O2+4NH3 6H2O+2N2;
6H2O+2N2;
②一定条件下,若反应中A、B和E的分子个数比为5:4:6,若A的个数是5,则B和E的分子个数比为4、6。
(1)物质的结构决定物质的性质,金属Na、Mg性质不同的原因是原子的最外层电子数不同;CO和CO2性质不同的原因是分子的构成不同;HCl、H2SO4可以使紫色石蕊试剂变红的原因是溶液中都含有氢离子。
(2)(ⅰ)从微观角度看,B图表示的分子是由一个氮原子和三个氢原子构成的,化学式是:NH3;
(ⅱ)从宏观角度看,图中CD物质是由不同种物质组成的,属于混合物。
(3)①F是氮气时其反应物是氧气与氨气,产物是水与氮气,其方程式是:3O2+4NH3 6H2O+2N2;
6H2O+2N2;
②一定条件下,若反应中A、B和E的分子个数比为5:4:6,若A的个数是5,则B和E的分子个数比为4、6,依据质量守恒定律可知,F为一氧化氮,化学式:NO。
故答为:(1)原子的最外层电子数不同; 分子的构成不同;溶液中都含有氢离子.
(2)(ⅰ)NH3;(ⅱ)CD;
(3)①3O2+4NH3 6H2O+2N2;②NO。
6H2O+2N2;②NO。

 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
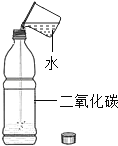
浙江新课程三维目标测评课时特训系列答案【题目】化学小组用如图所示自制装置进行“人体吸入和呼出气体成分”的探究。
(提出假设)人体呼出气体中二氧化碳的含量高于吸入气体
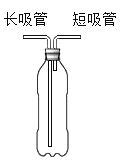
(进行实验)
实验 1
步骤 | 操作 | 现象 |
① | 在饮料瓶中装水至没过长吸管底端,对着短吸管缓慢吹气 | 水从长吸管端快速流出 |
② | 将饮料瓶中装满水,对着短管吹气,用排水法收集呼出气体,将燃着的木条快速伸入饮料瓶中 | 饮料瓶中木条熄灭 |
③ | 将水倒掉,向饮料瓶中加入澄清石灰水至没过长吸管底,从短吸管端吸气 30 秒,观察石灰水的变化;再从长吸管端吹气 30 秒, 观察石灰水的变化 |
(1)步骤①说明,自制装置的气密性_______(填“良好”或“不良”)。
(2)解释步骤①中出现相应实验现象的原因:______。
(3)步骤②中的现象_______(填“能”或“不能”)证明呼出气体中含二氧化碳,原因是______。
(4)若假设成立,步骤③中,预期会观察到的现象是_______。
实验2
实验1中有同学发现,吹气一段时间后发现,浑浊的石灰水重新变得澄清。他用上述装置加入与实验1等体积的石灰水,做下列实验来研究这一问题。
实验编号 | 石灰水浓度 | 持续吹气时间 | 瓶底现象 |
2﹣1 | 0.16% | 30 秒 | 澄清石灰水变浑浊 |
2﹣2 | 0.16% | 2 分钟 | 澄清石灰水先变浑浊,后又变得澄清 |
2﹣3 | 0.08% | 30 秒 | |
2﹣4 | 0.08% | 2 分钟 | 澄清石灰水先变浑浊,后又变得澄清 |
(反思与评价)
(5)能说明石灰水重新变澄清与石灰水浓度有关的实验是______(填实验编号)。
(6)实验Ⅰ中,吹气时间均为 30 秒,有同学观察到石灰水变澄清,而有的学生未观察到,产生现象差异的可能原因是________。