题目内容
【题目】某同学在做“氢气在空气中燃烧”实验时,对生成物的成分产生了质疑:水和过氧化氢具有相同的组成元素,那么氢气在空气中燃烧除生成水外,是否还有过氧化氢生成呢?带着疑问,该同学利用如图所示实验装置进行了以下探究。
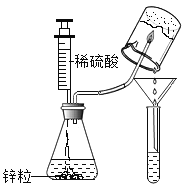
(提出猜想)氢气在空气中燃烧除生成水,还有过氧化氢生成。
(查阅资料)
①在一定条件下(低温环境下),氢气在空气中燃烧除生成水外,还有过氧化氢生成。
②过氧化氢溶液能使无色的淀粉碘化钾溶液变蓝色。
③低温时过氧化氢难分解
(实验探究)
主要步骤 | 主要现象 | 实验结论 |
Ⅰ.将注射器内的稀硫酸注入到盛有锌粒的锥形瓶中 | 在锌粒表面有______产生 | 反应的化学方程式为___________ |
Ⅱ.点燃经验纯后的氢气,用底部结有冰的小烧杯罩在火焰上方,用漏斗和试管收集所得液体。向试管中加入______。 | 氢气燃烧产生淡蓝色火焰,试管中液体由无色变_____色 | 氢气在空气中燃烧有过氧化氢生成 |
(反思评价)实验中将氢气燃烧的火焰对着冰,冰的作用是______。
A创设低温环境,使部分氢气燃烧产生一定量的过氧化氢
B使生成的过氧化氢溶入冰融化成的水中,便于收集
C有利于防止生成的过氧化氢分解
(拓展分析)除氢气和氧气反应会生成两种氧化物外,金属钠也具有类似的化学性质。钠常温露置在空气中与氧气反应生成氧化钠,钠在空气中燃烧生成过氧化钠(Na2O2);造成反应物相同,生成物不同的原因是________。
【答案】气泡 ![]() 无色的淀粉碘化钾溶液 蓝 ABC 反应条件(或者温度)
无色的淀粉碘化钾溶液 蓝 ABC 反应条件(或者温度)
【解析】
[实验探究]①锌与硫酸反应生成硫酸锌和氢气,所以在锌粒表面有气泡产生;反应的化学方程式为:Zn+H2SO4═ZnSO4+H2↑。
②由于过氧化氢溶液能使无色的淀粉碘化钾溶液变蓝色,氢气在空气中燃烧有过氧化氢生成,可以点燃经验纯后的氢气,用底部结有并冰的小烧杯罩在火焰上方,用漏斗和试管收集所得液体。向试管中加入无色的淀粉碘化钾溶液,试管中液体由无色变会变蓝色,说明氢气在空气中燃烧有过氧化氢生成;
[评价反思]实验中将氢气燃烧的火焰对着冰,冰创设低温环境,促使部分氢气燃烧产生一定量的过氧化氢,并冷却燃烧产生的气体,有利于生成的过氧化氢和较低的温度下溶入冰融化成的水中,便于收集;故选ABC。
[拓展分析] 钠常温露置在空气中与氧气反应生成氧化钠,钠在空气中燃烧生成过氧化钠(Na2O2);造成反应物相同,生成物不同的原因是反应条件(或者温度)。
故答案为:
[查阅资料]Ⅰ.气泡; Zn+H2SO4═ZnSO4+H2↑;Ⅱ.淀粉碘化钾溶液; 蓝。
[评价反思]ABC;[拓展分析]反应条件(或者温度)。

【题目】某白色固体可能由BaCl2、NaOH、Na2CO3、Na2SO4中的一种或几种物质组成,某兴趣小组同学为确定该白色固体的成分,进行了如下实验探究请你参与并回答相关问题。
I.初步探究:小明同学设计的实验过程及现象如图所示。
(查阅资料)BaCl2溶液显中性。
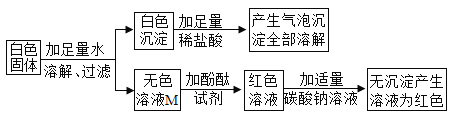
(初步结论)
(1)原白色固体中一定有的物质是_____。
(2)M溶液中的溶质一定有_____,一定没有BaCl2。
(交流讨论)小樱同学认为:无色溶液M变红色,说明溶液M中含有碱性物质,但不能由此推导出原固体物质中是否含有NaOH.若要进一步确定,需对溶液M继续进行探究。为此同学们进行了如下的探究:
Ⅱ.继续探究
(提出问題)无色溶液M中的碱性物质是什么?
(猜想与假设)猜想一:NaOH、Na2CO3;
猜想二:NaOH;
猜想三:_____。
(探究与结论)
实验步骤 | 实验现象 | 实验结论 |
A.取少量无色溶液M置于试管中,加入过量的BaCl2溶液,振荡,静置。 | _____ | 猜想一正确 |
B.取少量实验A所得上层清液置于试管中,加入_____。 | 溶液由无色变成红色 |
步骤A中加入过量的BaCl2溶液的目的是_____。在老师的指导下,同学们通过交流、讨论、实验,圆满完成了这次实验探究活动。