题目内容
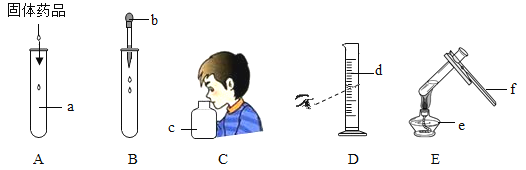
【题目】以下是实验室制取气体的常用仪器,回答下列问题:
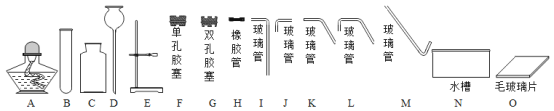
(1)标号为B的仪器名称是_____;
(2)实验室里,利用高锰酸钾制取氧气,并使用排水法收集。
①发生反应的化学方程式为_______;
②组装装置时,现有仪器B、C、E、F、H、K、M、N、O,还需补充的仪器是_____;
③若收集的氧气不纯,可能的原因:_______(一条即可);
(3)①制取0.4g ![]() ,理论上至少需要金属锌的质量为_____g;
,理论上至少需要金属锌的质量为_____g;
②组装制取氢气的发生装置时选择仪器D的优点是_____。
【答案】试管 ![]() A 一产生气泡就立即收集 13g 方便加液体药品
A 一产生气泡就立即收集 13g 方便加液体药品
【解析】
(1)标号为B的仪器名称是试管;
(2)实验室里,利用高锰酸钾制取氧气,发生装置是固体加热型;使用排水法收集如果一产生气泡就立即收集,这时的气体是装置中的空气,这样收集的氧气不纯;
(3)①利用化学方程式,根据![]() 质量计算金属锌的质量;
质量计算金属锌的质量;
②组装制取氢气的发生装置时选择仪器D长颈漏斗的优点是方便加液体药品。
(1)标号为B的仪器名称是试管;
(2)实验室里,利用高锰酸钾制取氧气,并使用排水法收集。
①高锰酸钾加热生成锰酸钾、二氧化锰、氧气,发生反应的化学方程式为![]() ;
;
②组装装置时,现有仪器B、C、E、F、H、K、M、N、O,反应需要加热,还需补充的仪器是酒精灯A;
③若收集的氧气不纯,可能的原因一产生气泡就立即收集,这时的气体是装置中的空气,这样收集的氧气不纯;
(3)①制取0.4g ![]() ,理论上至少需要金属锌的质量为
,理论上至少需要金属锌的质量为![]() ;
;
②组装制取氢气的发生装置时选择仪器D长颈漏斗的优点是方便加液体药品。

【题目】某白色固体可能由BaCl2、NaOH、Na2CO3、Na2SO4中的一种或几种物质组成,某兴趣小组同学为确定该白色固体的成分,进行了如下实验探究请你参与并回答相关问题。
I.初步探究:小明同学设计的实验过程及现象如图所示。
(查阅资料)BaCl2溶液显中性。
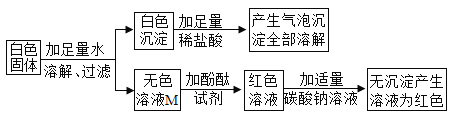
(初步结论)
(1)原白色固体中一定有的物质是_____。
(2)M溶液中的溶质一定有_____,一定没有BaCl2。
(交流讨论)小樱同学认为:无色溶液M变红色,说明溶液M中含有碱性物质,但不能由此推导出原固体物质中是否含有NaOH.若要进一步确定,需对溶液M继续进行探究。为此同学们进行了如下的探究:
Ⅱ.继续探究
(提出问題)无色溶液M中的碱性物质是什么?
(猜想与假设)猜想一:NaOH、Na2CO3;
猜想二:NaOH;
猜想三:_____。
(探究与结论)
实验步骤 | 实验现象 | 实验结论 |
A.取少量无色溶液M置于试管中,加入过量的BaCl2溶液,振荡,静置。 | _____ | 猜想一正确 |
B.取少量实验A所得上层清液置于试管中,加入_____。 | 溶液由无色变成红色 |
步骤A中加入过量的BaCl2溶液的目的是_____。在老师的指导下,同学们通过交流、讨论、实验,圆满完成了这次实验探究活动。