题目内容
【题目】某探究小组的同学对金属的性质很感兴趣,进行了如下探究。
(1)探究金属的活泼性。取等质量的A、B金属,分别投入溶质质量分数相同的足量的盐酸中,生成氢气的质量(m)与时间(t)的关系如图(已知A、B元素在生成物中的化合价相同)
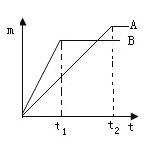
①由图分析,甲、乙、丙三位同学的对话正确的是(_____)
甲:时间t1时,产生氢气的质量A<B
乙:到时间t2时,金属均有剩余
丙:两种金属原子的相对原子质量A<B
②结论:金属A、B的活泼性 _______________。
(2)测定铜锌合金中铜的质量分数。向质量为26.0g的铜锌合金中滴入10%的稀硫酸98.0g时,恰好完全反应不再产生氢气。求
①生成氢气的质量_______________。
②合金中铜的质量分数_______________。
【答案】甲、丙 B强于A 0.2g 75%
【解析】
金属活动性顺序表中,在氢元素前面的金属能将氢元素从稀硫酸或盐酸中置换出来。
(1)取等质量的A、B金属,分别投入溶质质量分数相同的足量的盐酸中,金属完全反应,生成氢气的质量(m)与时间(t)的关系如图
①甲:时间t1时,产生氢气的质量A<B,对话正确;
乙:到时间t2时,不再产生氢气,说明金属完全反应,没有剩余,对话错误;
丙:A的价量比大于B的价量比,A、B元素在生成物中的化合价相同,两种金属原子的相对原子质量A<B,对话正确。故选甲丙。
②结论:B比A反应快,金属A、B的活泼性B强于A。
(2)
解:稀硫酸中溶质质量为的稀硫酸98.0g×10%=9.8g。

![]() ,x=0.2g,y=6.5g,
,x=0.2g,y=6.5g,
![]()
答:①生成氢气的质量0.2g;
②合金中铜的质量分数为75%。

 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案【题目】下表是某同学错题本中整理的部分内容,其中不需要修改的是( )
A化学用语 | B现象描述 | C性质与用途 | D物质鉴别 |
氧化铝—A12O3 H2—表示一个氢分子 Fe | 硫在氧气中燃烧—发出蓝紫色的火焰 红磷在空气中燃烧—产生大量的白烟 铁丝空气中燃烧—火星四射 | 氮气化学性质稳定——制氮肥 氦气密度小——填充探空气球 焦炭具有还原性——冶炼金属 | 鉴别硬水和软水—一加适量的肥皂水 鉴别CO2和CO——将气体通入澄清石灰水 鉴别黄铜和黄金——加适量的稀盐酸 |
A.AB.BC.CD.D