题目内容
【题目】根据下列甲、乙图示和相关叙述,回答下列问题:
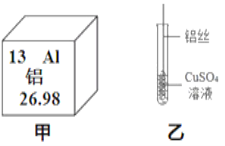
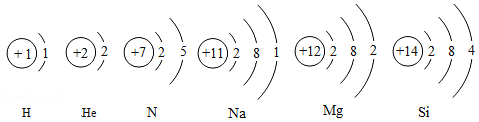
(1)图甲中铝元素的核电荷数为______,相对原子质量为______。
(2)铝块能制成铝箔是利用了铝的______(填“延展性”或“导电性”)。
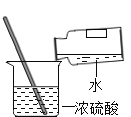
(3)图乙表示把一根用砂纸打磨过的铝丝插入硫酸铜溶液中,一段时间后,铝丝表面附着一层红色物质,溶液由蓝色逐渐变为无色,该反应的化学方程式为________,由此实验可以得出金属活动性顺序:铝______铜(填“>”、“<”或“=”)。
【答案】13; 26.98; 延展性; Cu; >
【解析】
(1)由元素周期表中元素信息可知,左上角的数字是原子序数,与原子的核电荷数相同,所以图甲中铝元素的核电荷数为13,故填13;
由元素周期表中元素信息可知,图中元素名称下方的数字就是原子的相对原子质量,所以铝原子的相对原子质量为26.98,故填26.98。
(2)铝具有良好的延展性,所以铝块能制成铝箔,故填延展性。
(3)由题文可知,铝与硫酸铜反应生成铜和硫酸铝,故反应的化学方程式写为:2Al+3CuSO4=Al2(SO4)3+3Cu;
由金属活动性的规律可知,活动性强的金属能将活动性弱的金属从其盐溶液中置换出来,铝能把硫酸铜溶液中的铜置换出来,说明铝的活动性比铜强,故填>。

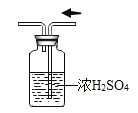
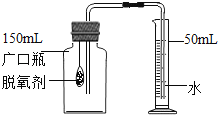
【题目】食品脱氧剂(以铁粉为主的物质组成)能通过化学反应除去密闭包装袋中的氧气,使食品处于无氧状态。张山同学用如图装置进行实验测定空气中氧气的含量。下表是张山同学在实验过程中记录的有关数据:
实验所需的时间/min | 0 | 5 | 10 | 30 | 35 | 45 |
量筒中液面的刻度/mL | 50 | 35 | 27.5 | 19.7 | 19.7 | 19.7 |
(1)脱氧剂发生复杂的化学反应,首先是铁粉与氧气、水反应生成氢氧化亚铁[Fe(OH)2]固体,写出该反应的符号表达式:_____。该反应属于_____反应(填基本反应类型)。
(2)实验过程中观察到量筒中的液面不断下降,水被吸入广口瓶中,出现该现象的原因是_____。
(3)分析表中数据得知,至少经过_____分钟后,量筒中的液面不再下降。
(4)根据表中实验数据进行推算,广口瓶中氧气的体积分数是_____(结果精确到0.1%)。
(5)小虎同学的实验用时45分钟,结果发现广口瓶中收集到的水约为张山同学的1/3,请你帮小虎同学找出造成实验失误的可能原因之一:_____。
【题目】用“盐酸--硫化钡法”生产BaCl2会产生有毒气体H2S,可用NaOH吸收H2S气体,同时又制取Na2S的方法进行处理(反应方程式为:H2S+2NaOH=Na2S+2H2O)。表为H2S回收工艺的各项生产成本:
项目 | 单价(元/吨) |
NaOH | 2500 |
Na2S | 5000 |
辅助费用(以处理1吨H2S计) | 1114 |
(1)若某化工厂每天用去10吨NaOH,理论上处理多少吨H2S?
(2)工业处理尾气需考虑经济效益和社会效益,结合上述资料,通过计算分析,单从经济效益考虑这种处理H2S的方法是盈利还是亏损。