题目内容
【题目】用“盐酸--硫化钡法”生产BaCl2会产生有毒气体H2S,可用NaOH吸收H2S气体,同时又制取Na2S的方法进行处理(反应方程式为:H2S+2NaOH=Na2S+2H2O)。表为H2S回收工艺的各项生产成本:
项目 | 单价(元/吨) |
NaOH | 2500 |
Na2S | 5000 |
辅助费用(以处理1吨H2S计) | 1114 |
(1)若某化工厂每天用去10吨NaOH,理论上处理多少吨H2S?
(2)工业处理尾气需考虑经济效益和社会效益,结合上述资料,通过计算分析,单从经济效益考虑这种处理H2S的方法是盈利还是亏损。
【答案】(1)4.25吨(2)盈利
【解析】
解:设10t NaOH处理的质量为x,同时生成Na2S的质量为y
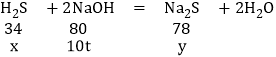
![]()
x=4.25t
y=9.75t
处理成本:4.25t×1114元/t+10t×2500元/t=29734.5元
Na2S收益:9.75t×5000元/t=48750元 48750元>29734.5元,盈利。
答:(1)若某化工厂每天用去10吨NaOH,理论上处理4.25吨H2S。
(2)单从经济效益考虑这种处理H2S的方法是盈利。
根据氢氧化钠的质量和对应化学方程式求算硫化氢的质量,进而求算对应的成本。
根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整。

【题目】加强对空气质量的监测是保护环境的一项重要措施,下表是某市2017年春夏秋冬空气监测平均数据,请你阅读后回答下列问题。
指标 指数 季节 | 可吸入颗粒物(PM10) | 氮氧化合物 (二氧化氮) | 二氧化硫 | 空气质量指标 |
春季 | 88 | 40 | 44 | Ⅱ |
夏季 | 67 | 33 | 36 | Ⅱ |
秋季 | 90 | 46 | 54 | Ⅱ |
冬季 | 98 | 69 | 60 | Ⅱ |
(1)某地空气污染指数为300以上,属于_____(填“中度”或“重度”)污染
(2)对该城市的空气质量影响最大的指标项目是_____,要对其加以防治的有效措施有_____(举一例)。
(3)该城市空气质量最好的季节是_____,可能原因之一是该季节绿叶茂盛,强化了_____。
(4)燃烧含硫的煤会生成二氧化硫,写出该反应的文字表达式:_____
【题目】在实验室制取氧气时,取MnO2和KClO3的固体混合物15.25g,加热至不再产生气体为止,收集到一定质量的氧气.某化学兴趣小组欲求得所制氧气的质量,他们将加热后剩余物冷却到一定温度后,通过多次加水测定剩余物质量的办法即可求出.加水的质量与剩余固体的质量见下表:(MnO2是不溶于水的固体粉末)
编号 | 1 | 2 | 3 | 4 |
加水的质量(g) | 10 | 10 | 10 | 10 |
剩余固体的质量(g) | 7.25 | 4.05 | m | 3 |
试求:(1)表中m值为______;
(2)混合物中KClO3的质量______;
(3)所制得氧气的质量______(写出具体计算过程).