题目内容
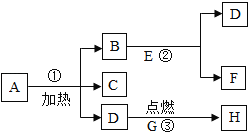
【题目】A、B……H八种物质,有如图所示关系:其中A是一种暗紫色固体,D能使带火星的木条复燃,F是一种最常见的液体,反应③火星四射,并且H是一种黑色的固体,在②的反应前后B的质量和化学性质均不改变。试推断:
(1)写出物质的化学式A_____、C_____。
写出物质的名称D_____、B_____。
(2)写出反应③的文字或符号表达式_____,反应基本类型_____。
【答案】KMnO4; K2MnO4; 氧气; 二氧化锰; 铁+氧气![]() 四氧化三铁; 化合反应;
四氧化三铁; 化合反应;
【解析】
根据气体D能使带火星的木条复燃,所以D是氧气,A是一种暗紫色固体,A加热会生成氧气,结合实验室制取氧气的药品和方法可知,A是高锰酸钾,在②的反应前后B的质量和化学性质均不改变,故B是二氧化锰,F是一种最常见的液体,F是水,则E是过氧化氢溶液,反应③火星四射,并且H是一种黑色的固体,则H是四氧化三铁,G是铁,则C是锰酸钾。
(1)由分析可知A、C的化学式分别为:KMnO4、K2MnO4;D、B的物质名称分别是氧气和二氧化锰;
(2)反应③是铁和氧气生成四氧化三铁的过程,其文字表达式为:铁+氧气![]() 四氧化三铁,化学方程式为:3Fe+2O2
四氧化三铁,化学方程式为:3Fe+2O2![]() Fe3O4,由两种或两种以上的物质发生化学反应生成另一种物质的反应是化合反应,该反应符合“多变一”的化合反应特征,属于化合反应。
Fe3O4,由两种或两种以上的物质发生化学反应生成另一种物质的反应是化合反应,该反应符合“多变一”的化合反应特征,属于化合反应。

【题目】在实验室制取氧气时,取MnO2和KClO3的固体混合物15.25g,加热至不再产生气体为止,收集到一定质量的氧气.某化学兴趣小组欲求得所制氧气的质量,他们将加热后剩余物冷却到一定温度后,通过多次加水测定剩余物质量的办法即可求出.加水的质量与剩余固体的质量见下表:(MnO2是不溶于水的固体粉末)
编号 | 1 | 2 | 3 | 4 |
加水的质量(g) | 10 | 10 | 10 | 10 |
剩余固体的质量(g) | 7.25 | 4.05 | m | 3 |
试求:(1)表中m值为______;
(2)混合物中KClO3的质量______;
(3)所制得氧气的质量______(写出具体计算过程).
【题目】某工厂用电解饱和食盐水的方法生产氯气、烧碱、氢气等化工产品(反应的化学方程式:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑),这种工业成为“氯碱工业”,某研究性学习小组对该厂生产的烧碱样品进行如下探究。
2NaOH+H2↑+Cl2↑),这种工业成为“氯碱工业”,某研究性学习小组对该厂生产的烧碱样品进行如下探究。
I.定性探究
(提出问题)烧碱样品中含有哪些杂质?
(猜想)猜想一:可能含有Na2CO3;
猜想二:可能含有NaCl,作出此猜想的依据______(用简洁的文字表述)。
(设计实验)
实验步骤 | 实验现象 | 解释或结论 |
①取适量烧碱样品置于试管中,加水溶解,并用手触摸试管外壁。 | 试管外壁发热 | 原因是 ______ |
②向①所得的溶液中加入稀硝酸至过量,将产生的气体通入澄清石灰水 | 有气体产生,澄清石灰水浑浊 | 样品中含有的杂质是 ______ |
③向②所得的溶液中滴加几滴硝酸银溶液。 | 无现象 | 猜想二 ______ (填“正确”或“错误”) |
(交流与讨论)小明同学提出:“上述实验中稀硝酸也可以用稀盐酸代替”,你同意他的观点吗?若不同意,写出理由______。
Ⅱ.定量探究
(提出问题)烧碱样品中氢氧化钠的质量分数是多少呢?
(设计实验)小丽同学设计探究方案①、②进行实验并测得数据如下:
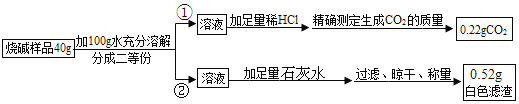
(交流与反思)
(1)小强同学认为方案②因缺少______(填操作名称),导致测得的氢氧化钠的质量分数偏小。
(2)请你利用方案①测得的数据计算烧碱样品中氢氧化钠的质量分数______(请在答题纸上写出计算过程)。