题目内容
【题目】化学是一门以实验为基础的学科,根据下图回答有关问题:
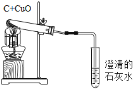
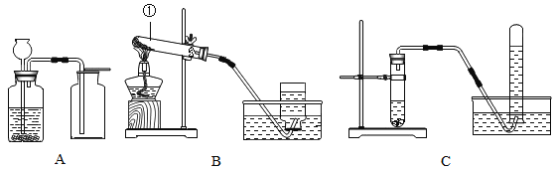
(1)上图是木炭还原氧化铜的反应,写出该反应的化学方程式_______________________;实验结束后要等冷却后再把试管里的粉末倒出,这样操作目的是_____________________;
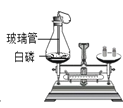
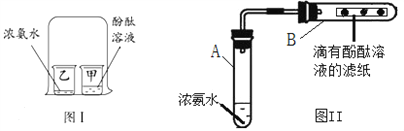
(2)上图为探究质量守恒定律的实验,该过程观察到的实验现象是___________________,请从微观角度解释反应前后天平平衡的的原因____________________________________;
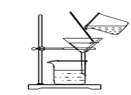
(3)上图中玻璃棒的作用是__________________________;实验得到的滤液仍然浑浊,原因是______(答一点即可);
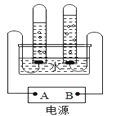
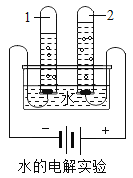
(4)上图为电解水装置,判断所接电源的正负极,图中A点表示_______极,该反应的化学方程式为___。
【答案】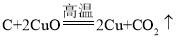 防止生成的铜重新被氧化 白磷燃烧产生大量白烟,放出热量,气球先变大后变小,天平平衡 化学反应前后,原子的种类、数目、质量保持不变 引流,防止液体飞溅 滤纸破损/仪器不干净/滤液高于滤纸边缘 负 2H2O
防止生成的铜重新被氧化 白磷燃烧产生大量白烟,放出热量,气球先变大后变小,天平平衡 化学反应前后,原子的种类、数目、质量保持不变 引流,防止液体飞溅 滤纸破损/仪器不干净/滤液高于滤纸边缘 负 2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
【解析】
(1)木炭高温条件下还原氧化铜反应原理:C+2CuO![]() 2Cu+CO2↑;实验结束后要等冷却后再把试管里的粉末倒出,因为未冷却的铜容易被空气中的氧气氧化生成氧化铜;
2Cu+CO2↑;实验结束后要等冷却后再把试管里的粉末倒出,因为未冷却的铜容易被空气中的氧气氧化生成氧化铜;
(2)白磷在空气中燃烧产生大量白烟,放出大量的热,锥形瓶中气体膨胀压强变大,气球先变大,待冷却后,锥形瓶中的气体被消耗,压强变小,气球也变小,天平平衡;所有的化学反应都符合质量守恒定律,化学反应前后,原子的种类、数目、质量保持不变;
(3)过滤操作时,玻璃棒有引流的作用;实验得到的滤液仍然浑浊,原因是:1滤纸破损2仪器不干净3滤液高于滤纸边缘;
(4)水通电实验中,正极产生氧气,负极产生氢气,氧气与氢气的体积比为1:2;图中A点连接的试管产生的气体多,是氢气,负极产生氢气,该反应的化学方程式为:2H2O![]() 2H2↑+O2↑。
2H2↑+O2↑。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】古人云“处处留心皆学问”,你若善于观察,就会获取更多的新知识。
(发现问题)在一次探究活动中,小强用塑料吸管向新制的澄清石灰水中吹气,在吹气的过程中发现石灰水先出现浑浊,后又变澄清,他感到很意外。于是小强又将纯净的二氧化碳通入新制的澄清石灰水中,观察到的现象与上次相同。
(1)请写出石灰水变浑浊的方程式________;小强做第二个实验的目的是________________。
(2)小强从老师那里得知:CO2能与CaCO3和H2O继续反应生成Ca(HCO3)2。由此,小强推测出Ca(HCO3)2的一条物理性质是能溶于水,写出CO2与CaCO3和H2O反应生成Ca(HCO3)2的化学方程式_________________________。
此外,小强还想了解Ca(HCO3)2的化学性质,提出了如下猜想:
(提出猜想)Ca(HCO3)2受热能否分解?
(查阅资料)Ca(HCO3)2受热分解生成CaCO3、H2O和CO2
(设计方案)小强用高锰酸钾制取氧气的发生装置来加热Ca(HCO3)2,加热时试管口要略_________倾斜,目的是__________________________________________。
(实验过程)小强在实验室找到一瓶Ca(HCO3)2粉末,取少量放入试管中进行加热,观察到试管口附近有小液滴产生。据此,小强得出结论:Ca(HCO3)2受热能够分解。
(反思评价)(1)小波认为小强的实验不能证明Ca(HCO3)2受热一定分解了,小波的理由是_______。
(2)请你设计实验方案,验证加热过程中有CO2产生。
选用试剂 | 实验操作方法 | 预想实验现象 | 结论 |
澄清石灰水 | 取适量Ca(HCO3)2粉末于试管中进行加热,将产生气体通入澄清石灰水中 | _________________ | 有CO2生成 |
(3)小红发现 CO2与CaCO3和H2O反应生成Ca(HCO3)2的化学反应方程式与Ca(HCO3)2受热分解的方程式在形式上近乎相反,于是联想到二氧化碳溶于水的过程也有类似情况,进行了如下课后小实验:
①将二氧化碳气体通入紫色石蕊溶液中,观察现象;
②将第①步实验得到的溶液置于酒精的火焰上加热,观察现象。
则下列选项中与小红进行的①②两步实验中石蕊溶液颜色变化情况相符是____(填字母)
A 紫色→红色→无色 B 红色→紫色→无色
C 红色→紫色→红色 D 紫色→红色→紫色
写出小红第①步实验中发生的反应的化学方程式_________________________,小红第②步实验中发生的化学反应属于__________反应(填反应类型)。