题目内容
【题目】原水(未作处理的水)中含有泥沙、悬浮物和细菌等杂质,氯气溶于水生成次氯酸(HClO)可杀死细菌。某水厂自来水的生产净化步骤如下:
![]()
(1)明矾溶于水后可以_______水中的悬浮杂质而沉降,起到一定的净水作用。
(2)用以除去水中细小固体颗粒的步骤为______(填序号,下同)。
(3)能消毒杀菌的步骤为______。
【答案】 吸附 C D
【解析】本题考查了自来水的生产过程和水的净化方法。
(1)明矾可将水中不溶性固体小颗粒吸附在一起,形成较大颗粒而加快沉降;
(2)加明矾、沉淀只能把固体杂质沉至水底,过滤才能除去水中在颗粒悬浮物杂质。故选C;
(3)加入氯气,氯气溶于水生成次氯酸(HClO)可杀死细菌,起到消毒杀菌的作用。故选择D;

 阅读快车系列答案
阅读快车系列答案【题目】在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化如图所示,下列说法不正确的是( )
物质 | 甲 | 乙 | 丙 | 丁 |
反应前物质的质量/g | 8 | 40 | 10 | 20 |
反应后物质的质量/g | 12 | 4 | X | 52 |
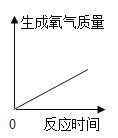
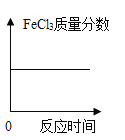
A. 反应中甲、乙的质量比为3:1 B. 该反应可以表示为2H2O ![]() 2H2↑+O2↑
2H2↑+O2↑
C. 该反应为分解反应 D. 丙可能为不参加反应的杂质
【题目】溶液在生产、生活中起着十分重要的作用。
(1)可作为溶质的是_______。
A.只有固体 B. 只有液体
C.只有气体 D. 气体、液体、固体都可以
(2)物质加入足量水中,能形成无色透明溶液的是_______。
A.汽油 B. 面粉 C. 纯碱 D. 硫酸铜
(3)物质加入水中形成溶液过程中,温度会升高的是_______。
A.烧碱 B. 氯化钠 D. 氧化钙 D. 碳酸钙
(4)下表是NaCl和KNO3在不同温度时的溶解度,回答问题。
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度g/100g水 | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 | |
①两种物质中,溶解度受温度影响变化较大的是__________。
②NaCl和KNO3溶解度相等的温度范围是__________。
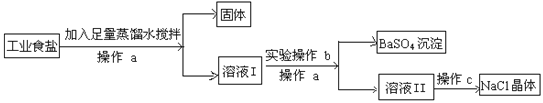
③KNO3晶体中含有少量NaCl,提纯KNO3晶体的方法是__________。
④60℃时,按图示操作:
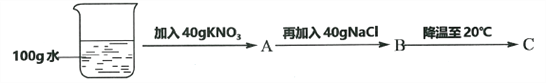
A中溶液是__________(填“饱和”或“不饱和”)溶液,C中溶液的总质量是__________g。
⑤50℃时,将两种物质的饱和溶液各100g,分别加热蒸发10g水后,再恢复到50℃,剩余溶液的质量:NaCl溶液__________(填“大于”“等于”或“小于”)KNO3溶液。