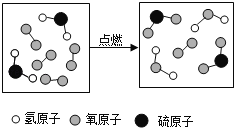
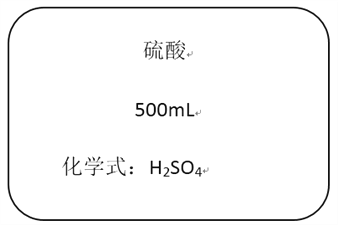
题目内容
【题目】如图是实验室制取气体的常用装置。
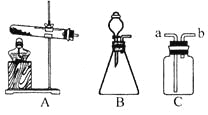
(1)A中的试管口为什么应略向下倾斜?
(2)写出选用B制取氧气的化学方程式。
(3)若采用C (气体由a口进入)收集到一种气体,请简述验证该气体的实验方法。
【答案】(1)防止试管口的冷凝水回流到热的试管底部,炸裂试管。
(2)2H2O2![]() 2H2O + O2↑
2H2O + O2↑
(3)将带火星的木条介入到集气瓶中,木条复燃,证明收集的气体是氧气。 (或向集气瓶中加入澄清的石灰水,石灰水变浑浊,证明收集的气体是二氧化碳。
【解析】试题分析:(1)A装置加热的是固体,固体中可能会有一些水分,加热时会形成水蒸气,试管口略向下倾斜的目的是防止试管口的冷凝水回流到热的试管底部,炸裂试管;
(2)B作为发生装置属于固液体常温下的反应,即采用的是过氧化氢制取氧气,反应的化学方程式为2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(3)采用C (气体由a口进入)收集到的气体,密度比空气大,可能是氧气也可能是二氧化碳,若是氧气,可将带火星的木条介入到集气瓶中,木条复燃,证明收集的气体是氧气;若是二氧化碳则向集气瓶中加入澄清的石灰水,石灰水变浑浊,证明收集的气体是二氧化碳。

【题目】兴趣小组的同学对碳酸氢钠、碳酸钠、氢氧化钠的某些性质进行相关探究.
【提出问题】它们溶液的酸碱性及与酸反应时溶液的pH如何变化?
【实验探究1】向等体积、等浓度的碳酸氢钠、碳酸钠、氢氧化钠溶液中,分别加入几滴紫甘蓝汁液,同时用蒸馏水进行对比实验,观察并记录现象如下:
液体名称 | 蒸馏水 | 碳酸氢钠溶液 | 碳酸钠溶液 | 氢氧化钠溶液 |
紫甘蓝汁液显示的颜色 | 蓝紫色 | 蓝色 | 绿色 | 黄色 |
查阅资料:
pH | 7.5~9 | 10~11.9 | 12~14 |
紫甘蓝汁液显示的颜色 | 蓝色 | 绿色 | 黄色 |
【得出结论1】三种溶液的碱性由强到弱的顺序为_____.
【实验探究2】甲同学在烧杯溶液中加入约5mL稀氢氧化钠溶液,滴入几滴酚酞溶液,此时溶液由_____色变为_____色.向其中加入稀盐酸,该反应的化学方程式为_____.
乙同学向一定体积、一定浓度的氢氧化钠溶液中,逐滴加入一定浓度的盐酸,得到pH变化与时间的关系如图1所示.
【得出结论2】从微观角度分析,该反应的实质是__________.
【实验探究3】向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入一定浓度的盐酸,得列pH变化与时间的关系如图2、图3所示.
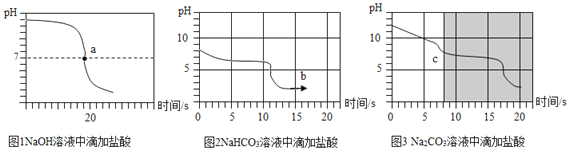
【交流与反思】b点的溶质为_____(写化学式),将图2和图3的阴影部分进行叠加,发现两者基本重合,c点的溶质_____(写化学式)
【得出结论3】通过上述分析,碳酸钠和盐酸反应过程,可以依次用以下两个化学方程式表示:_____________、____________.
【结论与反思】探究溶液的酸碱性及反应pH值的变化,可以认识反应的原理及进行的过程.