题目内容
【题目】(1)我国海盐年产量3千多万吨,居世界第一位,目前从海水中提取食盐的过程如图所示:
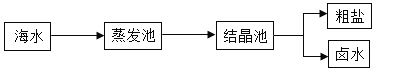
在上述过程中,下列说法不正确的是_______(填选项序号)。
A 水分蒸发所需能量主要为太阳能
B 在结晶池中主要通过降温结晶使氯化钠析出
C 风吹加速了水分的蒸发
D 当氯化钠晶体析出时,结晶池中的溶液为氯化钠的饱和溶液
(2)某学习小组的同学欲将粗盐进行初步提纯,进行了如下操作过程:
①取少量粗盐,加水搅拌至粗盐不再溶解;
②将步骤①所得混合液进行过滤,所使用的装置如下图所示;
③将步骤②所得滤液置于蒸发皿中加热蒸发,从而得到初步提纯后的精盐。
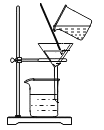
请指出(或改正)图中的一项错误_____________________________。
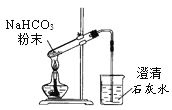
(3)1826年,比利时化学家索尔维发明了氨碱法制纯碱,以海水晒盐所得氯化钠为原料,配以水、氨气、二氧化碳制得纯碱。化学反应原理为:![]() ,
, ![]() .1926年,我国化学家侯德榜在氨碱法的基础上,创立了更为先进的联合制碱法(侯氏制碱法),是向滤出 NaHCO3晶体后的NH4C1溶液中加入NaCl粉末,析出可用作肥料的NH4Cl. NH4Cl和NaHCO3的溶解度曲线如图所示:
.1926年,我国化学家侯德榜在氨碱法的基础上,创立了更为先进的联合制碱法(侯氏制碱法),是向滤出 NaHCO3晶体后的NH4C1溶液中加入NaCl粉末,析出可用作肥料的NH4Cl. NH4Cl和NaHCO3的溶解度曲线如图所示:
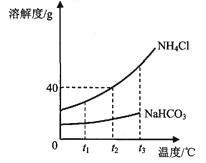
①当温度高于t3℃时, NaHCO3无溶解度数值,原因是____________________________;
②t2℃时,向200g水中加入40g氯化铵充分溶解,所得溶液是氯化铵的____溶液(填“饱和”、“不饱和之一);
③氨盐水吸收二氧化碳后生成NaHCO3和NH4Cl的过程中, NaHCO3首先从溶液中析出,原因是________填序号).
A 相同温度下, NaHCO3的溶解度小于NH4Cl B NaHCO3的溶解度受温度影响比氯化铵小
C NaHCO3的化学性质比氯化铵稳定 D 生成的 NaHCO3的质量比NH4Cl大
【答案】B 倾倒液体的烧杯没有紧靠在玻璃棒上 碳酸氢钠在高于t3℃时已经分解了 不饱和 A
【解析】
(1)
A.水分蒸发所需能量主要为太阳能,故正确;
B.在结晶池中主要通过蒸发水分结晶使氯化钠析出,故错误;
C.风吹加速了水分子的运动,也就加快了蒸发,故正确;
D.当氯化钠晶体析出时,结晶池中的溶液为氯化钠的饱和溶液,溶解不了才会析出,故正确;
故选B;
(2)过滤操作需要注意“一贴、两低和三靠”,由图示可知存在的错误是:倾倒液体的烧杯没有紧靠在玻璃棒上;
(3)
①据题目知碳酸氢钠的热稳定性差,当温读高于t3℃时,NaHCO3无溶解度数值,是因为碳酸氢钠在高于t3℃时已经分解了,故填:碳酸氢钠在高于t3℃时已经分解了;
②t2℃时,氯化铵的溶解度为40g,即t2℃时100g水加入40g氯化铵形成饱和溶液,故向200g水中加入40g氯化铵所得溶液是氯化铵的不饱和溶液,故填:不饱和;
③氨盐水吸收二氧化碳后生成NaHCO3和NH4Cl的过程中,NaHCO3首先从溶液中析出,是因为在相同温度下,NaHCO3的溶解度小于NH4Cl,故填:A。

 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
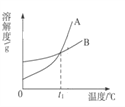
小学课堂作业系列答案【题目】KNO3和NaCl的溶解度表及溶解度曲线如右图,下列说法错误的是 ( )
温度/℃ | 0 | 20 | 40 | 60 | 80 | |
溶解度S/g | KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 |
NaCl | 35.7 | 36 | 36.6 | 37.3 | 38.4 | |
A. t1介于20℃-40℃之间
B. 50℃时,溶液的溶质质量分数:KNO3 >NaCl
C. 当KNO3中混有少量NaCl时,可用降温结晶的方法提纯KNO3
D. 60℃时,30g KNO3加入50g水,充分溶解,再降温到20℃,会析出晶体14.2g