题目内容
【题目】化学是在分子、原子层次上研究物质的科学。
(1)下列A~E是几种元素的粒子结构示意图或元素的信息,请回答:
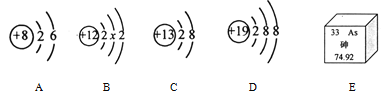
①B结构图中,x=________;砷的相对原子质量为_____________。
②A、C两元素形成化合物的化学式是___________。
③D元素的原子最外层电子数为__________。
(2)以下是二氧化碳转化为甲醇(CH3OH)的反应微观示意图:
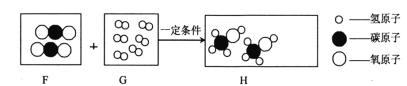
①请把H框内的粒子补画完整________。②该反应的化学方程式为________。
【答案】8 74.92 ![]() 1
1 ![]()
![]()
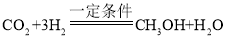
【解析】
(1)①原子核外电子排布规律,每层排2n2电子,故第二层排8个电子,故X=8;由元素信息图得,砷的相对原子质量为74.92;
②A为氧原子,易得到两个电子形成氧离子,化合价为-2价,、C为铝原子易失去三个电子形成铝离子,化合价为+3价,故形成的化合物的化学式为![]() 。
。
③原子核外电子数等于核内质子数,D元素的原子和核外电子排布为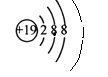 ,故最外层电子数为1;
,故最外层电子数为1;
(2)①根据质量守恒定律,H框内的粒子为:![]()
![]() ;
;
②反应的化学方程式为: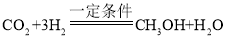

【题目】如图所示,在两支试管中进行实验,补全实验方案。
序号 | 目的 | 步骤或现象 |
A | 鉴别NaCl溶液和Na2CO3溶液 | ①试管1、2中分别加入两种溶液;②再向两支试管中加入_____。 |
B | 比较_____。 | ①试管1中加入一粒碘和5mL水;②试管2中加入一粒碘和5mL汽油。观察到1中固体几乎不溶解,2中固体全部溶解。 |
C | 比较锌、铁、铜的金属活动性 | ①试管1中加入ZnSO4溶液,试管2中加入CuSO4溶液; ②再分别向两支试管中插入铁丝。观察到的现象是_____。 |
【题目】在化学课上,甲同学将燃烧的钠迅速伸入到盛有CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上附粘附着白色物质。
(提出问题)黑色颗粒和白色物质是什么?
(进行猜想)甲认为黑色颗粒是_______,白色物质可能是Na2O或________;
乙同学还认为白色物质是氢氧化钠。
甲同学立刻认为乙同学的猜想是错误的,其理由是________。
(查阅资料)氧化钠、碳酸钠、硫酸钠均为白色固体,氧化钠溶于水生成氢氧化钠:Na2O+H2O=2NaOH,碳酸钠溶液显碱性。
(实验探究)甲同学对白色物质进行实验探究。
实验方案 | 实验作 | 实验现象 | 结 论 |
方案1 | 取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 | 溶液变成红色 | 白色物质为Na2O |
方案2 | ①取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液 | 出现白色沉淀 | 白色物质是_______。 |
②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
(反思评价)丙同学认为方案1得到的结论不正确,理由是_______。
(得出结论)钠在二氧化碳中燃烧的化学方程式为_______。通过以上探究,你还能获得哪些结论,请写出一条_______。
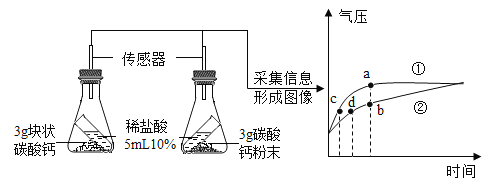
【题目】氢氧化钙久置会逐渐变质为碳酸钙。实验室有一瓶部分变质的氢氧化钙样品,为测定其中碳酸钙的质量分数,取16.2g样品于烧杯中,加足量的水,再将100g稀盐酸逐渐缓慢加入烧杯中并不断搅拌,获得相关数据如下表(提示:氢氧化钙先与盐酸反应时无气体产生),请回答问题并计算。
加入稀盐酸的质量/g | 20.0 | 40.0 | 60.0 | 80.0 | 100 |
生成CO2的质量/g | 0 | 2.2 | 4.4 | m | 5.5 |
(1)氢氧化钙变质是它与空气中的____________发生了反应。
(2)表中m的数值为_____________。
(3)试计算样品中碳酸钙的质量分数___________(请在答题卡上写出计算过程,计算结果精确到0.1%)。
(4)请在坐标中画出加入稀盐酸的质量与生成CO2的质量之间的变化关系图___________。

【题目】下列我国科技成果所涉及物质的应用中,体现物质物理性质的是
|
|
|
|
A 利用石墨烯优异的导电性,制成新型电阻触摸屏的电极 | B可燃冰是天然气水合物,作为新能源使用 | C 甲醇(CH3OH)低温制得氢气,用于新能源汽车 | D 优化煤的综合利用,发展煤制乙醇(C2H5OH)技术 |
A.AB.BC.CD.D