题目内容
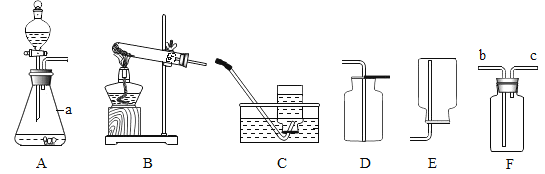
【题目】为探究金属的化学性质,兴趣小组使用等质量分数的稀盐酸进行如下实验。
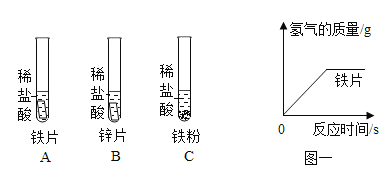
①A中反应的化学方程式是_____,由A、B反应的现象可推出Fe与Zn两种金属的活动性强弱是_____。
②通过比较B、C的反应现象,不能得出铁、锌两种金属的活动性强弱,原因是_____。
③充分反应后,B中固体全部消失,检验溶液中是否含有HCl,不可选择的药品是_____。
A Na2CO3固体
B AgNO3溶液
C CuO
D 铁粉
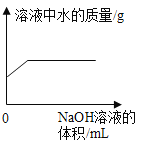
④A与C中分别放入等质量的铁片与铁粉,在图一中画出铁粉与稀盐酸反应时间与生成氢气的关系的图像_____。
【答案】![]() 锌的活动性比铁强 变量不唯一(片状和粉末接触面积不同,锌和铁金属种类不同,不能比较) B 图像中A是铁粉B是铁片
锌的活动性比铁强 变量不唯一(片状和粉末接触面积不同,锌和铁金属种类不同,不能比较) B 图像中A是铁粉B是铁片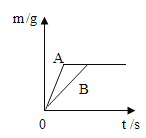
【解析】
①A中铁和盐酸反应生成氯化亚铁和氢气,反应的化学方程式是![]() ,由A、B反应的现象是锌片比铁片反应速度快,可推出Fe与Zn两种金属的活动性强弱是:锌的活动性比铁强。
,由A、B反应的现象是锌片比铁片反应速度快,可推出Fe与Zn两种金属的活动性强弱是:锌的活动性比铁强。
②通过比较B、C的反应现象,不能得出铁、锌两种金属的活动性强弱,原因是:变量不唯一(片状和粉末接触面积不同,锌和铁金属种类不同,不能比较金属的活动性)。
③锌和稀盐酸反应生成氯化锌和氢气。
A、Na2CO3固体和稀盐酸反应生成二氧化碳、水、氯化钠,有气泡生成,则有盐酸,没有气泡生成则没有盐酸,可以选择;
B 、AgNO3溶液和氯化锌反应生成氯化银白色沉淀,氯化锌干扰实验,不能选择;
C 、氧化铜和盐酸反应生成氯化铜蓝色溶液,生成蓝色溶液,有盐酸,没有生成蓝色溶液,没有盐酸,可以选择;
D、 铁粉和盐酸反应生成氯化亚铁和氢气,有气泡生成,则有盐酸,没有气泡生成则没有盐酸,可以选择;
故选B。
④A与C中分别放入等质量的铁片与铁粉,生成氢气质量相等,铁粉比铁片接触面积大,反应更快。图像中A是铁粉B是铁片

【题目】右图所示,某河旁甲、乙、丙、丁四座化工厂排放的工业废水中分别含有碳酸钠、氯化铜、氢氧化钠、盐酸中的一种.某同学对①、②、③、④处水质监测时记录了以下现象.根据现象推断,甲、乙、丙、丁四座化工厂排放工业废水的成分,错误的是( )
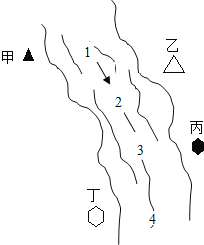
① | ② | ③ | ④ | |
记录现象 | 无色溶液 | 蓝色浑浊 | 浑浊消失 | 产生气泡 |
A.甲:碳酸钠 B.乙:氯化铜 C.丙:盐酸 D.丁:碳酸钠
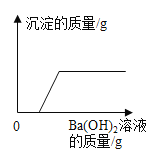
【题目】分析数据,获得信息实验室现有硫酸铜和硫酸钠的固体混合物样品,小明同学想测定样品中硫酸铜的质量分数。先称取该混合物样品 25g,完全溶于水中,然后取用了一定溶质质量分数的氢氧化钠溶液 100g 平均分四次加入其中,充分振荡,相关实验数据记录如下:
第1次 | 第2次 | 第3次 | 第4次 | |
加入氢氧化钠溶液的质量/g | 25 | 25 | 25 | 25 |
生成沉淀的质量/g | 4.9 | 9.8 | X | 14.7 |
请回答下列问题:
(1)上表中 X 的数值为_____________;
(2)计算原固体混合物样品中硫酸铜的质量分数为_____________? (写出计算步骤)
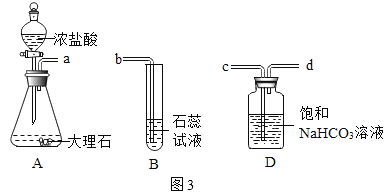
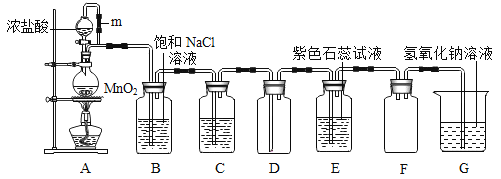
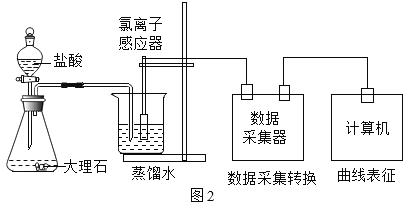
【题目】化学小组用图1装置验证二氧化碳与水的反应。

盐酸浓度 | 观察到的现象 | |
甲组 | 浓盐酸(36.5%) | B中石蕊溶液由紫色变成红色 C中石蕊溶液没有变为紫色 |
乙组 | 稀盐酸(13.5%) | B中石蕊溶液由紫色变为红色 C中石蕊溶液变为紫色 |
(1)A中反应的化学方程式为_____。
(2)乙组C中反应的化学方程式为_____。
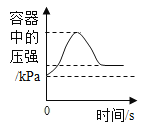
(讨论与交流)同学们认为甲组C中石蕊溶液没有变为紫色,是因为浓盐酸挥发出过多的HCl溶于石蕊溶液。
(提出猜想)盐酸的挥发性与浓度有关。
(进行实验)用图2装置研究不同浓度盐酸的挥发性。用离子传感器测定烧杯中所得溶液的氯离子浓度(氯离子浓度可以近似表示挥发出的HCl的量),实验数据见下表。
盐酸浓度与氯离子浓度的对应关系(相同时间内测得)
盐酸浓度(%) | 13.5 | 20 | 26.2 | 29.2 | 32.2 | 36.5 |
氯离子浓度(mg/L) | 1.1 | 1.4 | 3.7 | 19.0 | 59.8 | 209.2 |
分析表中数据,能够得出盐酸的挥发性与浓度的关系是_____。
(得出结论)猜想正确
(实验反思)甲组石蕊溶液变红不能证明二氧化碳与水反应。
(实验改进)甲组同学在装置A与装置B之间连接装置D。三个装置之间导管口的连接顺序是:a→_____ →_____→b。选择饱和NaHCO3溶液除杂的原因是_____。