题目内容
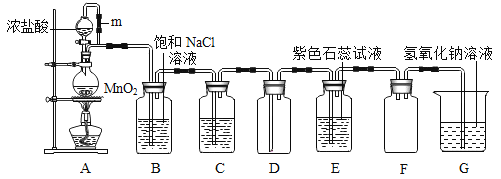
【题目】某校化学兴趣小组在实验室里用二氧化锰和浓盐酸在加热条件下制取氯气并进行有关氯气性质的实验探究(如图所示)。
(查阅资料)
Ⅰ、氯气(Cl2)是一种黄绿色的有毒气体,能溶于水,并能与水反应,反应的化学方程式为:![]() ;
;
Ⅱ、氯气溶于水所得的溶液为氯水,氯水除了具有消毒作用,HClO(次氯酸)还具有漂白作用;
Ⅲ、稀盐酸和二氧化锰不发生反应;
Ⅳ、氯气能与氢氧化钠溶液反应。
回答下列问题:
(1)A中m管的作用是_____;
(2)A是制取氯气的发生装置,除生成氯气外还有氯化锰(其中Mn为+2价)和一种常见氧化物,请写出其化学方程式_____;
(3)若进入装置D中的氯气是纯净干燥的,则装置B(饱和氯化钠溶液)的作用是_____,装置C中盛有的溶液是_____;
(4)装置E中石蕊溶液的颜色变化过程为:_____;
(5)①实验装置G的作用是_____;
②通过无数次实验和计算发现,取含溶质146g的浓盐酸和足量的二氧化锰反应,得到的氯气为_____(填字母)。
A 小于71g
B 等于71g
C 大于71g
D 等于35.5g
【答案】平衡烧瓶内外的压强,使分液漏斗中的液体顺利流下 ![]() 吸收氯化氢气体 浓硫酸 溶液由紫色变为红色,最终变成无色 吸收氯气,防止污染空气 A
吸收氯化氢气体 浓硫酸 溶液由紫色变为红色,最终变成无色 吸收氯气,防止污染空气 A
【解析】
(1)A中m管可以平衡烧瓶内外的压强,使分液漏斗中的液体顺利流下,故填平衡烧瓶内外的压强,使分液漏斗中的液体顺利流下。
(2)浓盐酸中含有氢元素与氯元素,二氧化锰中含有锰元素与氧元素,所以二者反应生成的常见氧化物是水,即浓盐酸与二氧化锰在加热的条件下反应生成氯化锰、氯气和水,故反应的化学方程式写为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
(3)浓盐酸具有挥发性,挥发出的氯化氢气体会干扰实验效果,氯化氢气体极易溶于水,装置B中的饱和氯化钠溶液能够吸收挥发出来的氯化氢气体,故填吸收氯化氢气体;
进入装置D中的氯气是纯净干燥的,则D装置中的作用是干燥气体,其中的干燥剂是浓硫酸,故填浓硫酸。
(4)干燥纯净的氯气进入E装置后与紫色石蕊试液中的水反应生成盐酸与次氯酸,盐酸呈酸性,能够使紫色石蕊试液变红,而次氯酸具有漂白性,能够将石蕊漂白成无色,故填溶液由紫色变为红色,最终变成无色。
(5)①氯气能与氢氧化钠溶液反应,装置G中的氢氧化钠溶液能够吸收残留的氯气,防止氯气污染空气,故填吸收氯气,防止污染空气;
②浓盐酸与二氧化锰能够反应生成氯气,随着反应的进行,浓盐酸的浓度逐渐减小,当浓盐酸变为稀盐酸时,反应不再发生,所以最终生成氯气的质量小于理论质量71g,故填A。

 阅读快车系列答案
阅读快车系列答案【题目】化学兴趣小组的同学将镁条放在热水中煮沸,趁热取出部分溶液,滴加酚酞试液,溶液变为红色,放置在空气中一段时间后,发现溶液的红色褪去。为了弄清楚红色褪去的原因进行了下列探究活动:查阅资料:镁可与热水反应生成氢气和氢氧化镁。该反应的化学方程式为_____。
三位同学分别对红色褪去的原因作出如下猜想:
甲:可能是实验所用的酚酞试液变质造成的;
乙:溶液可能与空气中的物质发生了反应;
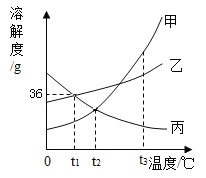
丙:氢氧化镁的溶解度随温度的降低而减小。
(1)同学们根据实验现象认为甲猜想不正确,理由是____。
(2)同学设计如下实验来验证乙猜想,实验记录如下表。
实验方法 | 实验现象 |
将上述红色溶液在空气中恒温放置一段时间 | 红色不褪去 |
将上述红色溶液在隔绝空气条件下恒温放置一段时间 | 红色不褪去 |
由该实验可知乙猜想______(填“正确”或“不正确”)
(3)若丙猜想是正确的,请设计实验证明,完成下表。
实验方法 | 实验现象 |
将上述红色溶液恒温放置一段时间 | 红色不褪去 |
____ | _____ |
(4)反思:
①请解释为什么在家里将自来水烧开倒入晾水杯中,开始杯中无沉淀物,一段时间后会在杯里看到白色沉淀物_____。
②请从微观角度解释为什么在热水中氢氧化镁可以使酚酞变红而在冷水中不可以_____。
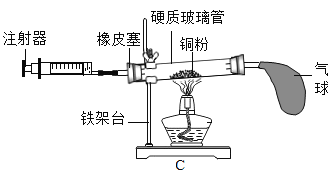
【题目】浓硫酸具有强腐蚀性,将碳与浓硫酸混合加热有气体产生,小明认为产生的气体可能是CO、CO2、SO2三种气体中的一种或多种,为此进行了,下列探究:
(查阅资料)
①SO2能使品红溶液褪色,易与高锰酸钾溶液反应而被吸收,能与氢氧化钠溶液反应,能使澄清石灰水变浑浊;
②CO和CO2均不能使品红溶液褪色,也不与高锰酸钾溶液反应。
(实验探究)为验证这三种气体,小明在老师的指导下,设计并进行如图所示实验:
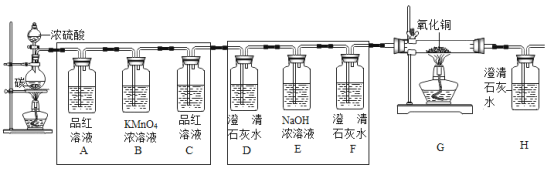
请完成如表:
实验现象 | 实验结论 |
装置A中品红溶液褪色 | 有__生成 |
__ | 有CO2生成 |
装置G中无明显现象 | __ |
(反思与评价)
(1)装置B中酸性高锰酸钾溶液的作用是__,若将装置A、D中的试剂交换,__(填“能”或“不能”)得出有CO2产生的结论。
(2)写出碳与浓硫酸反应的化学方程式__。